Note: Descriptions are shown in the official language in which they were submitted.
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
1
Procédé de fonctionnalisation de composés insaturés
Domaine de l'invention
L'invention porte sur un procédé de synthèse de composés fonctionnalisés, à
partir de
molécules insaturées. L'invention porte aussi sur l'utilisation de ces
composés en tant que
tensio-actifs, plastifiants, lubrifiants, monomères de polymères ou monomères
de
biopolymères etc.
Etat de la technique
La synthèse des composés à partir de molécules insaturées peut être effectuée
de plusieurs
façons. Elle peut être par exemple effectuée en deux étapes par la voie de
l'époxydation. La
première étape comprend une réaction d'époxydation par l'eau oxygénée en
présence d'un
acide carboxylique afin de former in situ un peracide qui constitue l'agent
d'époxydation. A
l'échelle industrielle, l'acide acétique est utilisé en présence d'un acide
minéral (H2SO4)
nécessaire afin de catalyser la formation du peracide. La deuxième étape
comprend la
réaction d'ouverture du cycle oxirane par un agent de clivage en présence d'un
système
catalytique acido-basique homogène.
Les catalyseurs homogènes fréquemment utilisés dans le cas de la réaction
d'ouverture
d'époxydes gras sont l'acide chlorhydrique, sulfurique, phosphorique,
fluoroborique ou
l'acide paratoluène sulfonique. Concernant la première étape, le peracide est
la cause
principale des réactions secondaires d'ouverture du cycle oxirane lors du
processus
industriel, ce qui engendre une sélectivité en époxydes gras rarement
supérieure à 80 %. De
plus, l'acide minéral dans un environnement oxydant cause de graves problèmes
de
corrosion, ce qui peut avoir des conséquences sur l'utilisation, le stockage,
et le transport.
Concernant la deuxième étape, les catalyseurs homogènes utilisés doivent être
neutralisés,
ce qui nécessite des étapes supplémentaires très souvent productrices de
déchets. Ces
technologies entraînent de nombreuses réactions secondaires qui ont
incontestablement un
impact négatif sur la sélectivité de la réaction.
La présente invention a pour objet de remédier à au moins un des inconvénients
cités ci-
dessus.
Bref résumé de l'invention
La présente invention concerne un procédé de synthèse de composés de formule
(la) ou
(lb), un stéréo-isomère, un mélange de ceux-ci, un oligomère et/ou un polymère
de ceux-ci :
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
2
R5
L1/ R \
"1
) _______________________________ 0 6 0
0 OR6
R 0 0
Ri
( R3 Ri ( R3
R2
R4
R2)
R4
(la) (lb)
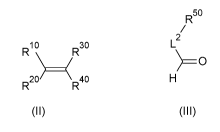
comprenant la réaction d'un composé de formule (II) avec de l'oxygène
atmosphérique ou
moléculaire, en présence d'au moins un aldéhyde de formule (III), et
facultativement en
5 présence d'au moins un catalyseur ou d'au moins un initiateur de radicaux
;
R50
R R
i o L2
3 0
0
RR40 H
(Il) (III)
dans lesquelles :
R1 est H ou est choisi parmi le groupe comprenant alkyle en Cl-020, alcényle
en 02-020, et
aryle en 06-012, chaque groupe étant éventuellement substitué par un ou
plusieurs
groupements, identiques ou différents, choisis parmi le groupe comprenant un
atome
d'halogène, -OH, -CHO, oxo, cyano, -NR92, époxy, alkoxy en Cl-04, alkyle en 01-
06, aryle en
06-012, -000L1R5, -000R8, et -0O2R60 ;
R2 est H, cyano ou un atome d'halogène, ou est choisi parmi le groupe
comprenant alkyle en
01-020, alcényle en 02-020, aryle en 06-012, et 06-C12arylalkyle en 01_6,
chaque groupe étant
éventuellement substitué par un ou plusieurs groupements, identiques ou
différents, choisis
parmi le groupe comprenant un atome d'halogène, -OH, -CHO, oxo, cyano, -NR92,
époxy,
alkoxy en 01-04, alkyle en Cl-06, aryle en 06-012, -000L1R5, -000R8, et -
002R60;
R3 est choisi parmi le groupe comprenant époxy, -000R8, -0O2R8, alkyle en Cl-
020, alcényle
en 02-020, aryle en 06-012, et C6-C12arylalkyle en Ci_6, chaque groupe étant
éventuellement
substitué par un ou plusieurs groupements, identiques ou différents, choisis
parmi le groupe
comprenant un atome d'halogène, -OH, -CHO, oxo, cyano, -NR92, époxy, alkoxy en
Cl-04,
alkyle en Cl-06, aryle en 06-012, -000L1R5, -000R8, et -002R60;
R4 est H, cyano, un atome d'halogène, ou est choisi parmi le groupe comprenant
alkyle en
01-020, alcényle en 02-020, et aryle en 06-012, chaque groupe étant
éventuellement substitué
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
3
par un ou plusieurs groupements, identiques ou différents, choisis parmi le
groupe
comprenant un atome d'halogène, -OH, -CHO, oxo, cyano, -NR92, époxy, alkoxy en
Cl-04,
alkyle en Cl-06, aryle en 06-012, -000L1R5, -000R8, et -0021e;
ou bien R1 et R3 peuvent former, avec les carbones auxquels ils sont liés, un
groupe choisi
parmi un cycloalkyle en 05-012 et un cycloalcényle en 05-012, chaque groupe
étant
éventuellement substitué par un ou plusieurs groupements, identiques ou
différents, choisis
parmi le groupe comprenant un atome d'halogène, -OH, oxo, cyano, époxy, -
000L1R6, -
000R8, -002R60, alkyle en 01-06, hydroxyalkyle en 01-06, et alcényle en 02-06;
R5 est choisi parmi le groupe comprenant H, un atome d'halogène, -OH, -CHO,
époxy, -SR8,
cyano, nitro, isocyanate, alkyle en Cl-020, alkoxy en 01-04, alcényle en 02-
020, alcynyle en
02-020, hétérocycloalkyle, -002R8, et -NR92 ;
R6 est H ou -00-L1-R6 ;
12 est une liaison covalente simple, ou est choisi parmi le groupe comprenant
alkylène en Cl-
020, cycloalkylène en 03-012, alcénylène en 02-012, cycloalcénylène en 05-012,
arylène en
06-012, hétéroarylène, et hétérocycloalkylène, chaque groupe étant
éventuellement substitué
par un ou plusieurs groupements, identiques ou différents, choisis parmi le
groupe
comprenant un atome d'halogène, -OH, oxo, nitro, -CHO, -000L1R6, -002R60, -
NR92, alkyle
en Cl-06, alkoxy en Cl-04, aryle en 06-012, _ 06-C12aryloxy, 06-C12arylalkyle
en 0l-6,
hydroxyalkyle en Cl-06, et C1_6alkylaryle en 06-012;
R1 est H, ou est choisi parmi le groupe comprenant alkyle en Cl-020, alcényle
en 02-020, et
aryle en 06-012, chaque groupe étant éventuellement substitué par un ou
plusieurs
groupements, identiques ou différents, choisis parmi le groupe comprenant un
atome
d'halogène, -OH, -CHO, oxo, cyano, -NR92, époxy, alkoxy en Cl-04, -000L2R66,
alkyle en
Cl-06, aryle en 06-012, -000R8, et -002R6 ;
R2 est H, cyano, un atome d'halogène, ou -CHO, ou est choisi parmi le groupe
comprenant
alkyle en Cl-020, alcényle en 02-020, aryle en 06-012, et 06-C12arylalkyle en
0l_6, chaque
groupe étant éventuellement substitué par un ou plusieurs groupements,
identiques ou
différents, choisis parmi le groupe comprenant un atome d'halogène, -OH, -CHO,
oxo,
cyano, -NR92, époxy, alkoxy en Cl-04, -000L2R50, alkyle en Cl-06, aryle en 06-
012, -000R5,
et -002R60;
R3 est choisi parmi le groupe comprenant époxy, -000R5, -002R5, alkyle en Cl-
020,
alcényle en 02-020, aryle en 06-012, et 06-C12arylalkyle en 0l_6, chaque
groupe étant
éventuellement substitué par un ou plusieurs groupements, identiques ou
différents, choisis
parmi le groupe comprenant un atome d'halogène, -OH, -CHO, oxo, cyano, -NR92,
époxy,
alkoxy en 01-04, -000L2R50, alkyle en 01-06, aryle en 06-012, -000R5, et -
002R6 ;
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
4
R4 est H, cyano, un atome d'halogène, ou -CHO, ou est choisi parmi le groupe
comprenant
alkyle en Cl-020, alcényle en 02-020, et aryle en 06-012, chaque groupe étant
éventuellement
substitué par un ou plusieurs groupements, identiques ou différents, choisis
parmi le groupe
comprenant un atome d'halogène, -OH, -CHO, oxo, cyano, -NR92, époxy, alkoxy en
Cl-04,
-00OL2R5 , alkyle en 01-06, aryle en 06-012, -000R8, et -002R80;
ou bien R1 et R3 peuvent former, avec les carbones auxquels ils sont liés,
un groupe choisi
parmi un cycloalkyle en 06-012 ou un cycloalcényle en 06-012, chaque groupe
étant
éventuellement substitué par un ou plusieurs groupements, identiques ou
différents, choisis
parmi le groupe comprenant un atome d'halogène, -OH, -CHO, cyano, oxo, époxy, -
000R8,
-002R80, -000L2R50, alkyle en 01-06, hydroxyalkyle en 01-06, et alcényle en 02-
06;
R5 est choisi parmi le groupe comprenant H, -CHO, époxy, un atome d'halogène,
-OH, -SR8,
cyano, nitro, isocyanate, alkyle en Cl-020, alkoxy en Cl-04, alcényle en 02-
020, alcynyle en
02-020, hétérocycloalkyle, -002R8, et -NR92 ;
L2 est une liaison covalente simple, ou est choisi parmi le groupe comprenant
alkylène en
Cl-Cm, cycloalkylène en 03-012, alcénylène en 02-012, cycloalcénylène en 06-
012, arylène en
06-012, hétéroarylène, et hétérocycloalkylène, chaque groupe étant
éventuellement substitué
par un ou plusieurs groupements, identiques ou différents, choisis parmi le
groupe
comprenant un atome d'halogène, oxo, nitro, -CHO, -OH, -NR92, alkyle en Cl-06,
alkoxy en
06-C12arylalkyle en 01-6, C1_6alkylaryle en 06-012, 06-C12aryloxy,
hydroxyalkyle en
01-06, et aryle en 06-012;
R8 est choisi parmi les groupes comprenant H ou alkyle en Cl-06
éventuellement substitué
par un ou plusieurs groupements, identiques ou différents, choisis parmi le
groupe
comprenant -OH, -CHO, -0-COR7, et alkyle en Cl-06;
R7 est choisi parmi le groupe comprenant alkyle en Cl-024, alcényle en 02-020,
et aryle en
06-012, chaque groupe étant éventuellement substitué par un ou plusieurs
groupements,
identiques ou différents, choisis parmi le groupe comprenant -OH, époxy et -
000L1R5 ;
R8 est choisi parmi le groupe H ou alkyle en Cl-06; et R9 est choisi parmi le
groupe H, alkyle
en Cl-06, ou aryle en 06-012.
Le procédé selon la présente invention tire son originalité, par rapport aux
procédés actuels,
dans la réduction des étapes de synthèse ainsi que dans la méthode de synthèse
envisagée.
Les réactions chimiques impliquées dans le procédé selon l'invention utilisent
comme agent
de transformation l'oxygène, ce qui évite d'une part les risques liés au
stockage et au
transport de l'eau oxygénée (traditionnellement utilisée pour la fabrication
des époxydes) et
d'autre part réduit considérablement le coût de production puisque l'oxygène
peut être
prélevé dans l'air ambiant (oxygène atmosphérique). Selon un mode de
réalisation préféré,
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
pour être menée à bien dans ces conditions, la synthèse nécessite la présence
d'un solide
minéral (catalyseur). Selon un mode de réalisation préféré, le catalyseur joue
un rôle
essentiel puisque d'une part il accélère les réactions chimiques, il diminue
leur demande
énergétique et d'autre part il simplifie considérablement le procédé de
fabrication. Le présent
5 procédé permet une synthèse plus propre pour un coût de fabrication
moindre. Les
composés multifonctionnels produits par la réaction appelés aussi monomères
peuvent
aussi réagir entre eux lors de la réaction pour donner des dimères qui à
leur tour peuvent
réagir avec les différents monomères pour donner des oligomères (tri,
quadrimères, etc) très
variés, et des polymères.
L'invention propose donc un procédé original, économique et écologique de
production de
composés multifonctionnels, ces derniers pouvant être à la base de la
production de produits
très divers et notamment de matière plastique ou de lubrifiant, etc. Les
molécules
synthétisées, sont particulièrement avantageuses comme synthons pour la
fabrication de
matière plastique. Avantageusement, les molécules synthétisées peuvent être
elles même
des oligomères ou des polymères. Différents types de polymères peuvent être
envisagés
suivant la nature de la fonction greffée par le procédé de synthèse. Lorsque
le composé
insaturé et/ou aldéhydique utilisé dans le procédé est issu du monde végétal
(esters d'acides
gras), les matières plastiques ou polymères fabriqués en aval du procédé de
synthèse seront
donc produits au départ d'une matière première renouvelable, ils sont donc
qualifiés de
biopolymères ou encore bio based polymers .
La présente invention concerne aussi un composé de formule (le) ou (If), un
stéréo-isomère
de celui-ci, ou un mélange de ceux-ci ;
1 7 1 8
R 16 R 16
0R1 8
0 R1 7
0R1 9 0 R1 9
(le)
dans lesquelles :
R16 est H ou est choisi parmi le groupe comprenant -00-(CR21R22)q_R23, -CO-
aryle en 06-012,
et -CO-cycloalcényle en 05-012, chaque groupe étant éventuellement substitué
par un ou
plusieurs groupements, identiques ou différents, choisis parmi le groupe
comprenant un
atome d'halogène, -OH, -000R19, -0O2R24, et alkyle en Cl-06;
R17 est choisi parmi le groupe comprenant un alkyle en 02-020 et un alcényle
en 02-020,
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
6
chaque groupe étant éventuellement substitué par un ou plusieurs groupements,
identiques
ou différents, choisis parmi le groupe comprenant un alkyle en Cl-06, un aryle
en 06, -0R18
et -002R24;
R18 est H ou est choisi parmi le groupe comprenant un alkyle en 02-020 et un
alcényle en
C2-Co, chaque groupe étant éventuellement substitué par un ou plusieurs
groupements,
identiques ou différents, choisis parmi le groupe comprenant un alkyle en 01-
06, un aryle en
06, -0R18 et -002R24;
ou bien R17 et R18 peuvent former, avec les carbones auxquels ils sont liés,
un groupe choisi
parmi un cycloalkyle en 05-012 ou un cycloalcényle en 05-012, chaque groupe
étant
éventuellement substitué par un ou plusieurs groupements, identiques ou
différents, choisis
parmi le groupe comprenant un atome d'halogène, -0R16, -000R19, -002R24, et
alkyle en
Cl-06;
R19 est choisi parmi le groupe comprenant -(0R21R22)q_R23, un aryle en 06-012,
et un
cycloalcényle en 05-012, chaque groupe étant éventuellement substitué par un
ou plusieurs
groupements, identiques ou différents, choisis parmi le groupe comprenant un
atome
d'halogène, -OH, -000R19, -002R24, et alkyle en 01-06;
q est un indice entier compris entre 3 et 12 ;
chaque R21 identique ou différent est choisi parmi H ou un alkyle en 01-06;
chaque R22 identique ou différent est choisi parmi H ou un alkyle en 01-06;
R23 est H ou -OH, ou est choisi parmi le groupe comprenant un alkyle en 01-06
et un aryle en
06-012, chaque groupe étant éventuellement substitué par un ou plusieurs
groupements,
identiques ou différents, choisis parmi le groupe comprenant un atome
d'halogène, -OH,
-000R19, -002R24, et alkyle en 01-06;
R24 est H ou un alkyle en 01-06 éventuellement substitué par un ou plusieurs
groupements,
identiques ou différents, choisis parmi le groupe comprenant -OH, -0-COR25, et
alkyle en
01-06; et
R25 est choisi parmi le groupe comprenant alkyle en 02-020, et alcényle en 02-
020, chaque
groupe étant éventuellement substitué par un ou plusieurs groupements,
identiques ou
différents, choisis parmi le groupe comprenant -OH, époxy, -0R16, et -000R19.
Selon un mode de réalisation préférée la présente invention concerne aussi un
composé de
formule (le) ou (If), un stéréo-isomère de celui-ci, ou un mélange de ceux-ci
; à la condition
que le composé ne soit pas le 9-(hexanoyloxy)-10-hydroxyoctadecanoate de
méthyle, le 1 0-
(hexanoyloxy)-9-hydroxyoctadecanoate de méthyle, l'ester octanoïque de
l'hydroxyoléate de
méthyle, l'ester 2-éthyl-hexyl de l'hydroxyoléate de méthyle,
l'hydroxybenzoyloxy-
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
7
octadodecanéate de méthyle, 1,2-heptanediol dicaproate et le 1,2-octanediol
dicaproate.
La présente invention concerne aussi l'utilisation des composés selon
l'invention, dans la
préparation de polymères, de biopolymères, de tensio-actifs, de plastifiants,
de lubrifiants ou
de biocides. De préférence, l'invention concerne l'utilisation des composés
selon l'invention,
dans la préparation de polymères ou de biopolymères. La présente invention
concerne aussi
l'utilisation d'un composé selon l'invention, comme monomère pour la
préparation de
polyuréthane.
D'autres aspects, particularités et avantages de la présente invention
apparaîtront à la
lecture de la description qui va suivre et des exemples qui l'illustrent
donnés simplement à
titre d'illustration et qui ne sauraient en aucune façon limiter la portée de
l'invention.
Brève description des figures
La figure 1 représente un graphique montrant les courbes cinétiques de
conversion en
réactifs et de rendement en produits dans le cas de la réaction de l'hexanal
avec le 4-octène
dans l'exemple 3.
La figure 2 représente un graphique montrant l'évolution de la composition du
milieu
réactionnel en fonction du temps pour la réaction de l'exemple 4.
La figure 3 représente les spectres infrarouges du produit fonctionnalisé de
l'exemple 5 en
présence de di-isocyanate avant polymérisation (t = 0 min) et après
polymérisation (t=240
min).
La figure 4 représente les spectres infrarouges du produit fonctionnalisé de
l'exemple 6
avant polymérisation (t = 0 min) et après polymérisation (t = 30 min).
La figure 5 représente un graphique montrant la sélectivité en produits
fonctionnalisés en
fonction du rendement pour les catalyseurs testés à l'exemple 7.
Description détaillée de l'invention
Selon un premier aspect, la présente invention concerne un procédé de synthèse
de
composés multifonctionnels : comprenant la réaction d'un composé de formule
(II) avec de
l'oxygène atmosphérique ou moléculaire, en présence d'au moins un aldéhyde de
formule
(III), et facultativement en présence d'au moins un catalyseur ou d'au moins
un initiateur de
radicaux ;
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
8
R50
R R0
i o L2
3
) __ 0
RR40 H
(Il) (III)
dans lesquelles :
R1 est H, ou est choisi parmi le groupe comprenant alkyle en Cl-020, alcényle
en 02-020, et
aryle en 06-012, chaque groupe étant éventuellement substitué par un ou
plusieurs
groupements, identiques ou différents, choisis parmi le groupe comprenant un
atome
d'halogène, -OH, -CHO, oxo, cyano, -NR92, époxy, alkoxy en 01-04, -000L2R50,
alkyle en
01-06, aryle en 06-012, -000R8, et -002R60;
R2 est H, cyano, un atome d'halogène, ou -CHO, ou est choisi parmi le groupe
comprenant
alkyle en Cl-020, alcényle en 02-020, aryle en 06-012, et 06-C12arylalkyle en
0l_6, chaque
groupe étant éventuellement substitué par un ou plusieurs groupements,
identiques ou
différents, choisis parmi le groupe comprenant un atome d'halogène, -OH, -CHO,
oxo,
cyano, -NR92, époxy, alkoxy en 01-04, -000L2R50, alkyle en Cl-06, aryle en 06-
012, -000R8,
et -002R80;
R3 est choisi parmi le groupe comprenant époxy, -000R8, -002R8, alkyle en Cl-
020,
alcényle en 02-020, aryle en 06-012, et 06-C12arylalkyle en 0l_6, chaque
groupe étant
éventuellement substitué par un ou plusieurs groupements, identiques ou
différents, choisis
parmi le groupe comprenant un atome d'halogène, -OH, -CHO, oxo, cyano, -NR92,
époxy,
alkoxy en Cl-04, -000L2R50, alkyle en Cl-06, aryle en 06-012, -000R8, et -
002R60;
R4 est H, cyano, un atome d'halogène, ou -CHO, ou est choisi parmi le groupe
comprenant
alkyle en Cl-020, alcényle en 02-020, et aryle en 06-012, chaque groupe étant
éventuellement
substitué par un ou plusieurs groupements, identiques ou différents, choisis
parmi le groupe
comprenant un atome d'halogène, -OH, -CHO, oxo, cyano, -NR92, époxy, alkoxy en
Cl-04,
-000L2R50, alkyle en Cl-06, aryle en 06-012, -000R8, et -002R6 ;
ou bien R1 et R3 peuvent former, avec les carbones auxquels ils sont liés,
un groupe choisi
parmi un cycloalkyle en 05-012 ou un cycloalcényle en 05-012, chaque groupe
étant
éventuellement substitué par un ou plusieurs groupements, identiques ou
différents, choisis
parmi le groupe comprenant un atome d'halogène, -OH, -CHO, cyano, oxo, époxy, -
000R8,
-002R80, -000L2R50, alkyle en Cl-06, hydroxyalkyle en Cl-06, et alcényle en 02-
06;
R5 est choisi parmi le groupe comprenant H, -CHO, époxy, un atome d'halogène,
-OH, -SR8,
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
9
cyano, nitro, isocyanate, alkyle en Cl-020, alkoxy en 01-04, alcényle en 02-
020, alcynyle en
02-020, hétérocycloalkyle, -002R8, et -NR92 ;
L2 est une liaison covalente simple, ou est choisi parmi le groupe comprenant
alkylène en
01-020, cycloalkylène en 03-012, alcénylène en 02-012, cycloalcénylène en 05-
012, arylène en
C6-C12, hétéroarylène, et hétérocycloalkylène, chaque groupe étant
éventuellement substitué
par un ou plusieurs groupements, identiques ou différents, choisis parmi le
groupe
comprenant un atome d'halogène, oxo, nitro, -CHO, -OH, -NR92, alkyle en 01-06,
alkoxy en
01-04, C6-C12arylalkyle en C1-6, C6-C12aryloxy, C1_6alkylaryle en 06-012,
hydroxyalkyle en
Cl-06, et aryle en 06-012;
R8 est choisi parmi les groupes comprenant H et alkyle en Cl-06
éventuellement substitué
par un ou plusieurs groupements, identiques ou différents, choisis parmi le
groupe
comprenant -OH, -CHO, -0-COR7, et alkyle en Cl-06;
R7 est choisi parmi le groupe comprenant alkyle en Cl-024, alcényle en 02-020,
et aryle en
06-012, chaque groupe étant éventuellement substitué par un ou plusieurs
groupements,
identiques ou différents, choisis parmi le groupe comprenant -OH, époxy et -
000L1R8 ;
R8 est choisi parmi le groupe H ou alkyle en Cl-06; et
chaque R9 identique ou différent est choisi parmi le groupe H, alkyle en Cl-
06, ou aryle en
06-012.
De préférence, la présente invention concerne un procédé de synthèse selon le
premier
aspect dans lequel le ou les composés multifonctionnels est un composé de
formule (la) ou
(lb), un stéréo-isomère, un mélange de composés de cette famille, et/ou un
oligomère et/ou
un polymère de ceux-ci.
La présente invention concerne de préférence un procédé de synthèse des
composés de la
famille représentée par la formule (la) ou (lb), un stéréo-isomère, un mélange
de composés
de cette famille, et/ou un oligomère et/ou un polymère de ceux-ci, tels que
les composés de
formule (1c) ou (Id),
R5
5
Li/
) _______________________________ 0
0
6
R0
0
\
\
RI
(la)
R3
R2/ \R4
R2/
R4
(la) (lb)
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
R3 R4 R2 1
R60 R60
0 0
R2 R4
p
L
(1c) (Id)
comprenant la réaction d'une molécule insaturée de formule (II) avec de
l'oxygène
atmosphérique ou moléculaire, en présence d'au moins un aldéhyde de formule
(III) et
5 facultativement en présence d'au moins un catalyseur ou d'au moins un
initiateur de
radicaux ; dans lesquelles :
p est un indice entier compris entre 1 et 10 000, de préférence p est un
indice entier compris
entre 1 et 1000, par exemple p est un indice entier compris entre 1 et 100;
R1 est H ou est choisi parmi le groupe comprenant alkyle en Cl-020, alcényle
en 02-020, et
10 aryle en 06-012, chaque groupe étant éventuellement substitué par un ou
plusieurs
groupements (par exemple 1, 2, 3, ou 4), identiques ou différents, choisis
parmi le groupe
comprenant un atome d'halogène, -OH, -CHO, oxo, cyano, -NR92, époxy, alkoxy en
Cl-04,
alkyle en 01-06, aryle en 06-012, -000L1R5, -000R8, et -002R60; de préférence
R1 est H ou
est choisi parmi le groupe comprenant alkyle en 01-020, alcényle en 02-020, et
aryle en
06-012, chaque groupe étant éventuellement substitué par 1, 2 ou 3
groupements, identiques
ou différents, choisis parmi le groupe comprenant -OH, -CHO, oxo, cyano, -
NR92, époxy,
alkoxy en Cl-04, alkyle en Cl-06, aryle en 06-012, -000L1R5, -000R8, et -
002R60; de
préférence R1 est H ou est choisi parmi le groupe comprenant alkyle en Cl-020,
et alcényle
en 02-020, chaque groupe étant éventuellement substitué par 1, 2 ou 3
groupements,
identiques ou différents, choisis parmi le groupe comprenant -OH, oxo, alkoxy
en Cl-02,
alkyle en 01-06, -000L1R5, et -002R60; de préférence R1 est H ou est choisi
parmi le groupe
comprenant alkyle en 01-012, et alcényle en 02-012, chaque groupe étant
éventuellement
substitué par 1, 2 ou 3 groupements, identiques ou différents, choisis parmi
le groupe
comprenant -OH, alkyle en Cl-06, -000L1R5, et -002R60;
R2 est H, cyano, ou un atome d'halogène, ou est choisi parmi le groupe
comprenant alkyle
en Cl-020, alcényle en 02-020, aryle en 06-012, et 06-C12arylalkyle en Cl-6,
chaque groupe
étant éventuellement substitué par un ou plusieurs groupements (par exemple 1,
2, 3, ou 4),
identiques ou différents, choisis parmi le groupe comprenant un atome
d'halogène, -OH,
-CHO, oxo, cyano, -NR92, époxy, alkoxy en Cl-04, alkyle en Cl-06, aryle en 06-
012,
-000L1R5, -000R8, et -002R60; de préférence R2 est H ou est choisi parmi le
groupe
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
11
comprenant alkyle en Cl-020, alcényle en 02-020, aryle en 06-012, et C6-
C12arylalkyle en 01_6,
chaque groupe étant éventuellement substitué par 1, 2 ou 3 groupements,
identiques ou
différents, choisis parmi le groupe comprenant -OH, -CHO, époxy, oxo, cyano, -
NR92, alkoxy
en 01-04, alkyle en 01-06, aryle en 06-012, -000L1R5, -000R8, et -002R60; de
préférence R2
est H ou est choisi parmi le groupe comprenant alkyle en Cl-020, et alcényle
en 02-020,
chaque groupe étant éventuellement substitué par 1, 2 ou 3 groupements,
identiques ou
différents, choisis parmi le groupe comprenant oxo, alkoxy en Cl-02, alkyle en
Cl-06,
-000L1R5, et -002R60; de préférence R2 est H ou est choisi parmi le groupe
comprenant
alkyle en Cl-012, et alcényle en 02-012, chaque groupe étant éventuellement
substitué par 1,
2 ou 3 groupements, identiques ou différents, choisis parmi alkyle en Cl-06, -
000L1R5, ou
-002R60; de préférence R2 est H ou un alkyle en Cl-012, éventuellement
substitué par 1, 2
ou 3 groupements, identiques ou différents, choisis parmi alkyle en Cl-06, -
000L1R5, ou
-002R60' de préférence R2 est H;
R3 est choisi parmi le groupe comprenant époxy, -000R8, -002R8, alkyle en Cl-
020, alcényle
en 02-020, aryle en 06-012, et 06-C12arylalkyle en 01_6, chaque groupe étant
éventuellement
substitué par un ou plusieurs groupements (par exemple 1, 2, 3, ou 4),
identiques ou
différents, choisis parmi le groupe comprenant un atome d'halogène, -OH, -CHO,
oxo,
cyano, -NR92, époxy, alkoxy en Cl-04, alkyle en Cl-06, aryle en 06-012, -
000L1R5, -000R8,
et -002R60; de préférence R3 est choisi parmi le groupe comprenant alkyle en
Cl-020,
alcényle en 02-020, et aryle en 06-012, chaque groupe étant éventuellement
substitué par 1,
2 ou 3 groupements, identiques ou différents, choisis parmi le groupe
comprenant -OH,
-CHO, oxo, époxy, alkoxy en Cl-04, alkyle en Cl-06, aryle en 06-012, -000L1R5
et -002R60;
de préférence R3 est choisi parmi le groupe comprenant alkyle en Cl-020, et
alcényle en
02-020, chaque groupe étant éventuellement substitué par 1, 2 ou 3
groupements, identiques
ou différents, choisis parmi le groupe comprenant -OH, oxo, alkoxy en Cl-02,
alkyle en
Cl-06, -000L1R5 et -002R60 ; de préférence R3 est choisi parmi le groupe
comprenant alkyle
en Cl-012, et alcényle en 02-012, chaque groupe étant éventuellement substitué
par 1, 2 ou 3
groupements, identiques ou différents, choisis parmi -OH, alkyle en Cl-06, -
000L1R5 ou
-002R6 ;
R4 est H, cyano, ou un atome d'halogène, ou est choisi parmi le groupe
comprenant alkyle
en Cl-020, alcényle en 02-020, et aryle en 06-012, chaque groupe étant
éventuellement
substitué par un ou plusieurs groupements (par exemple 1, 2, 3, ou 4),
identiques ou
différents, choisis parmi le groupe comprenant un atome d'halogène, -OH, -CHO,
oxo,
cyano, -NR92, époxy, alkoxy en Cl-04, alkyle en Cl-06, aryle en 06-012, -
000L1R5, -000R8,
et -002R6 ; de préférence R4 est H, ou est choisi parmi le groupe comprenant
alkyle en
Cl-020, alcényle en 02-020, et aryle en 06-012, chaque groupe étant
éventuellement substitué
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
12
par 1, 2 ou 3 groupements, identiques ou différents, choisis parmi le groupe
comprenant
-OH, -CHO, oxo, époxy, alkoxy en Cl-04, alkyle en 01-06, aryle en 06-012, -
000L1R5, et
-002R60; de préférence R4 est H, ou est choisi parmi le groupe comprenant
alkyle en 01-020,
et alcényle en 02-020, chaque groupe étant éventuellement substitué par 1, 2
ou 3
groupements, identiques ou différents, choisis parmi le groupe comprenant oxo,
alkoxy en
Cl-02, alkyle en Cl-06, -000L1R5, et -002R66 ; de préférence R4 est H, ou est
choisi parmi le
groupe comprenant alkyle en Cl-012, et alcényle en 02-012, chaque groupe étant
éventuellement substitué par 1, 2 ou 3 groupements, identiques ou différents,
choisis parmi
alkyle en 01-06, -000L1R5, ou -002R60; de préférence R4 est H ou alkyle en 01-
012,
éventuellement substitué par 1, 2 ou 3 groupements, identiques ou différents,
choisis parmi
alkyle en 01-06, -000L1R5, ou -002R66 ; de préférence R4 est H;
ou bien R1 et R3 peuvent former, avec les carbones auxquels ils sont liés, un
groupe choisi
parmi un cycloalkyle en 05-012 ou un cycloalcényle en 05-012, chaque groupe
étant
éventuellement substitué par un ou plusieurs groupements (par exemple 1, 2, 3,
ou 4),
identiques ou différents, choisis parmi le groupe comprenant un atome
d'halogène, -OH, oxo,
cyano, époxy, -000L1R5, -000R8, -002R66,alkyle en 01-06, hydroxyalkyle en 01-
06, et
alcényle en 02-06; de préférence ou bien R1 et R3 peuvent former, avec les
carbones
auxquels ils sont liés, un groupe choisi parmi un cycloalkyle en 05-012 ou un
cycloalcényle
en 05-012, chaque groupe étant éventuellement substitué 1, 2, 3 ou 4
groupements,
identiques ou différents, choisis parmi le groupe comprenant un -OH, oxo,
époxy, -000L1R5,
-000R8, -002R60, alkyle en Cl-06, et alcényle en 02-06 de préférence ou bien
R1 et R3
peuvent former, avec les carbones auxquels ils sont liés, un groupe choisi
parmi un
cycloalkyle en 05-010 ou un cycloalcényle en 05-010, chaque groupe étant
éventuellement
substitué par 1, 2, ou 3 groupements, identiques ou différents, choisis parmi -
OH, époxy,
alkyle en 01-06, ou alcényle en 02-06;
R5 est choisi parmi le groupe comprenant H, un atome d'halogène, -OH, -CHO,
époxy, -SR8,
cyano, nitro, isocyanate, alkyle en 01-020, alkoxy en 01-04, alcényle en 02-
020, alcynyle en
02-020, hétérocycloalkyle, -002R8, et -NR92 ; de préférence R5 est choisi
parmi le groupe
comprenant Cl, F, I, Br, -OH, -SH, -CHO, époxy, cyano, nitro, isocyanate,
alkoxy en Cl-04,
alcényle en 02-012, alcynyle en 02-012, hétérocycloalkyle, -002R8, et -NR92 ;
de préférence,
R5 est choisi parmi le groupe comprenant Cl, F, I, Br, -OH, -CHO, époxy, -SH,
cyano, et
nitro ; de préférence -OH, -SH, époxy, cyano ou nitro ; de préférence -OH, -
SH, époxy ou
cyano;
R6 est H ou -0O-L1-R5;
L1 est une liaison covalente simple, ou est choisi parmi le groupe comprenant
alkylène en
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
13
Cl-020, cycloalkylène en 03-012, alcénylène en 02-012, cycloalcénylène en 05-
012, arylène en
06-012, hétéroarylène, et hétérocycloalkylène, chaque groupe étant
éventuellement substitué
par un ou plusieurs groupements (par exemple 1, 2, 3, ou 4), identiques ou
différents, choisis
parmi le groupe comprenant un atome d'halogène, -OH, oxo, nitro, -CHO, -
000L1R5,
-002R60, -NR92, alkyle en 01-06, alkoxy en 01-04, aryle en 06-012, 06-
C12aryloxY,
06-C12arylalkyle en 01_6, hydroxyalkyle en 01-06, et C1_6alkylaryle en 06-012;
de préférence
12 est une liaison covalente simple, ou est choisi parmi le groupe comprenant
alkylène en
Cl-020, cycloalkylène en 03-012, cycloalcénylène en 05-012, et arylène en 06-
012, chaque
groupe étant éventuellement substitué par 1, 2, 3, ou 4 groupements,
identiques ou
différents, choisis parmi le groupe comprenant un atome d'halogène, -OH, oxo, -
CHO,
-000L1R5, -002R60, -NR92, alkyle en Cl-06, alkoxy en 01-04, hydroxyalkyle en
Cl-06, et aryle
en 06-012; de préférence 12 est une liaison covalente simple, ou est choisi
parmi le groupe
comprenant alkylène en Cl-011, cycloalkylène en 03-012, et arylène en 06-012,
chaque
groupe étant éventuellement substitué par 1, 2, 3, ou 4 groupements,
identiques ou
différents, choisis parmi le groupe comprenant un atome d'halogène, -OH, -CHO,
-000L1R5,
-002R60, alkyle en Cl-06, et aryle en 06-012; de préférence 12 est une liaison
covalente
simple, ou est un alkylène en Cl-011, ou un cycloalkylène en 03-012;
éventuellement
substitué par 1, 2, ou 3, groupements, identiques ou différents, choisis parmi
le groupe
comprenant un atome d'halogène, -OH, -CHO, -000L1R5, -002R60, alkyle en Cl-06,
et aryle
en 06-012;
R1 est H, ou est choisi parmi le groupe comprenant alkyle en Cl-020, alcényle
en 02-020, et
aryle en 06-012, chaque groupe étant éventuellement substitué par un ou
plusieurs
groupements (par exemple 1, 2, 3, ou 4), identiques ou différents, choisis
parmi le groupe
comprenant un atome d'halogène, -OH, -CHO, oxo, cyano, -NR92, époxy, alkoxy en
Cl-04,
-000L2R50, alkyle en Cl-06, aryle en 06-012, -000R8, et -002R60; de préférence
R1 est H,
ou est choisi parmi le groupe comprenant alkyle en Cl-020, alcényle en 02-020,
et aryle en
06-012, chaque groupe étant éventuellement substitué par 1, 2, ou 3
groupements,
identiques ou différents, choisis parmi le groupe comprenant -OH, -CHO, oxo,
cyano, -NR92,
époxy, alkoxy en Cl-04, -000L2R50, alkyle en Cl-06, aryle en 06-012, -000R8,
et -002R60;
de préférence R1 est H, ou est choisi parmi le groupe comprenant alkyle en Cl-
020, et
alcényle en 02-020, chaque groupe étant éventuellement substitué par 1, 2, ou
3
groupements, identiques ou différents, choisis parmi le groupe comprenant -OH,
-CHO, oxo,
-000L2R50, alkoxy en Cl-02, alkyle en Cl-06, et -002R60; de préférence R1 est
H, ou est
choisi parmi le groupe comprenant alkyle en Cl-012, et alcényle en 02-012,
chaque groupe
étant éventuellement substitué par 1, 2 ou 3 groupements, identiques ou
différents, choisis
parmi -CHO, oxo, alkyle en Cl-06, -000L2R50, et -002R60; de préférence R1 est
H, ou est
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
14
choisi parmi le groupe comprenant alkyle en Cl-012, et alcényle en 02-012,
chaque groupe
étant éventuellement substitué par 1, 2 ou 3 groupements, identiques ou
différents, choisis
parmi -CHO, oxo, alkyle en 01-06, ou -000L2R50 ;
R2 est H, cyano, un atome d'halogène, ou -CHO, ou est choisi parmi le groupe
comprenant
alkyle en 01-020, alcényle en 02-020, aryle en 06-012, et 06-C12arylalkyle en
01-6, chaque
groupe étant éventuellement substitué par un ou plusieurs groupements (par
exemple 1, 2,
3, ou 4), identiques ou différents, choisis parmi le groupe comprenant un
atome d'halogène,
-OH, -CHO, oxo, cyano, -NR92, époxy, alkoxy en Cl-04, -000L2R50, alkyle en Cl-
06, aryle en
06-012, -000R8, et -002R60; de préférence R2 est H ou -CHO ou est choisi
parmi le groupe
comprenant alkyle en Cl-020, alcényle en 02-020, et aryle en 06-012, chaque
groupe étant
éventuellement substitué par 1, 2, ou 3 groupements, identiques ou différents,
choisis parmi
le groupe comprenant -OH, -CHO, oxo, cyano, -NR92, époxy, alkoxy en Cl-04, -
000L2R50
,
alkyle en Cl-06, aryle en 06-012, 000R8, et -002R60; de préférence R2 est H
ou -CHO, ou
est choisi parmi le groupe comprenant alkyle en Cl-020, et alcényle en 02-020,
chaque
groupe étant éventuellement substitué par 1, 2, ou 3 groupements, identiques
ou différents,
choisis parmi -OH, oxo, -CHO, -000L2R50, alkoxy en Cl-02, ou alkyle en Cl-06;
de
préférence R2 est H ou -CHO, ou est choisi parmi le groupe comprenant alkyle
en Cl-012, et
alcényle en 02-012, chaque groupe étant éventuellement substitué par 1, 2, ou
3
groupements, identiques ou différents, choisis parmi -CHO, alkyle en Cl-06, ou
-000L2R50;
R3 est choisi parmi le groupe comprenant époxy, -000R8, -002R8, alkyle en Cl-
020,
alcényle en 02-020, aryle en 06-012, et 06-C12arylalkyle en 0l-6, chaque
groupe étant
éventuellement substitué par un ou plusieurs groupements (par exemple 1, 2, 3,
ou 4),
identiques ou différents, choisis parmi le groupe comprenant un atome
d'halogène, -OH,
-CHO, oxo, cyano, -NR92, époxy, alkoxy en Cl-04, -000L2R50, alkyle en Cl-06,
aryle en
06-012, -000R8, et -002R60; de préférence R3 est choisi parmi le groupe
comprenant
époxy, alkyle en Cl-020, alcényle en 02-020, et aryle en 06-012, chaque groupe
étant
éventuellement substitué par 1, 2 ou 3 groupements, identiques ou différents,
choisis parmi
le groupe comprenant -OH, alkyle en Cl-06, -CHO, oxo, époxy, alkoxy en Cl-04, -
000L2R50
,
aryle en 06-012, -000R8, et -002R60; de préférence R3 est choisi parmi le
groupe
comprenant alkyle en Cl-020, et alcényle en 02-020, chaque groupe étant
éventuellement
substitué par 1, 2 ou 3 groupements, identiques ou différents, choisis parmi
oxo, alkoxy en
Cl-02, alkyle en Cl-06, -CHO, -000L2R5 ou -002R60 ; de préférence R3 est
choisi parmi le
groupe comprenant alkyle en Cl-012, et alcényle en 02-012, chaque groupe étant
éventuellement substitué par 1, 2 ou 3 groupements, identiques ou différents,
choisis parmi
alkyle en Cl-06, -CHO, -000L2R5 ou -002R60;
R4 est H, cyano, un atome d'halogène, ou -CHO, ou est choisi parmi le groupe
comprenant
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
alkyle en Cl-020, alcényle en 02-020, et aryle en 06-012, chaque groupe étant
éventuellement
substitué par un ou plusieurs groupements (par exemple 1, 2, 3, ou 4),
identiques ou
différents, choisis parmi le groupe comprenant un atome d'halogène, -OH, -CHO,
oxo,
cyano, -NR92, époxy, alkoxy en 01-04, -000L2R50, alkyle en 01-06, aryle en 06-
012, -000R8,
5 et -002R80; de préférence R4 est H ou -CHO, ou est choisi parmi le
groupe comprenant
alkyle en Cl-020, alcényle en 02-020, et aryle en 06-012, chaque groupe étant
éventuellement
substitué par 1, 2 ou 3 groupements, identiques ou différents, choisis parmi
le groupe
comprenant -OH, oxo, époxy, alkoxy en 01-04, alkyle en Cl-06, aryle en 06-012,
-000L2R50
,
et -002R60; de préférence R4 est H ou -CHO, ou est choisi parmi le groupe
comprenant
10 alkyle en Cl-020, et alcényle en 02-020, chaque groupe étant
éventuellement substitué par 1,
2 ou 3 groupements, identiques ou différents, choisis parmi le groupe
comprenant oxo alkoxy
en Cl-02, alkyle en Cl-06, -000L2R50, et -002R80 ; de préférence R4 est H ou -
CHO, ou est
choisi parmi le groupe comprenant alkyle en Cl-012, et alcényle en 02-012,
chaque groupe
étant éventuellement substitué par 1, 2 ou 3 groupements, identiques ou
différents, choisis
15 parmi alkyle en Cl-06, -000L2R50, ou -002R60;
de préférence R4 est H, -CHO ou alkyle en Cl-012, éventuellement substitué
par 1, 2 ou 3
groupements, identiques ou différents, choisis parmi alkyle en Cl-06, -
000L2R50, ou
-002R80; de préférence R4 est H ou -CHO;
ou bien R1 et R3 peuvent former, avec les carbones auxquels ils sont liés,
un groupe choisi
parmi un cycloalkyle en 05-012 ou un cycloalcényle en 05-012, chaque groupe
étant
éventuellement substitué par un ou plusieurs groupements (par exemple 1, 2, 3,
ou 4),
identiques ou différents, choisis parmi le groupe comprenant un atome
d'halogène, -OH,
-CHO, cyano, oxo, époxy, -000R8, -002R80, -000L2R50, alkyle en 01-C6
hydroxyalkyle en
Cl-06, et alcényle en 02-06; de préférence ou bien R1 et R3 peuvent former,
avec les
carbones auxquels ils sont liés, un groupe choisi parmi un cycloalkyle en 05-
012 ou un
cycloalcényle en 05-012, chaque groupe étant éventuellement substitué par 1,
2, 3, ou 4
groupements, identiques ou différents, choisis parmi le groupe comprenant -OH,
-CHO, oxo,
époxy, -000L2R50, alkyle en Cl-06, et alcényle en 02-06; de préférence ou bien
R1 et R3
peuvent former, avec les carbones auxquels ils sont liés, un groupe choisi
parmi un
cycloalkyle en 05-010 ou un cycloalcényle en 05-010, chaque groupe étant
éventuellement
substitué par 1, 2, ou 3 groupements, identiques ou différents, choisis parmi
le groupe
comprenant -OH, -CHO, époxy, alkyle en Cl-06, et alcényle en 02-06;
R5 est choisi parmi le groupe comprenant H, -CHO, époxy, un atome d'halogène,
-OH, -SR8,
cyano, nitro, isocyanate, alkyle en Cl-020, alkoxy en Cl-04, alcényle en 02-
020, alcynyle en
C2-Co, hétérocycloalkyle, -002R8, et -NR92 ; de préférence R5 est choisi
parmi le groupe
comprenant Cl, F, I, Br, -OH, -CHO, époxy, -SH, cyano, nitro, isocyanate,
alkoxy en Cl-04,
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
16
alcényle en 02-012, alcynyle en 02-012, hétérocycloalkyle, -0O2R8, et -NR92 ;
de préférence,
R5 est choisi parmi le groupe comprenant Cl, F, I, Br, -OH, -CHO, -SH, cyano,
et nitro, de
préférence -OH, -CHO, -SH, époxy, cyano ou nitro, de préférence -OH, -SH ou
cyano;
L2 est une liaison covalente simple, ou est choisi parmi le groupe comprenant
alkylène en
Cl-020, cycloalkylène en 03-012, alcénylène en 02-012, cycloalcénylène en 06-
012, arylène en
06-012, hétéroarylène, et hétérocycloalkylène, chaque groupe étant
éventuellement substitué
par un ou plusieurs groupements (par exemple 1, 2, 3, ou 4), identiques ou
différents, choisis
parmi le groupe comprenant un atome d'halogène, oxo, nitro, -CHO, -OH, -NR92,
alkyle en
alkoxy en 01-04, C6-C12arylalkyle en 01_6, C1_6alkylaryle en 06-012, C6-
C12aryloxY,
hydroxyalkyle en 01-06, et aryle en 06-012 ; de préférence L2 est une liaison
covalente
simple, ou est choisi parmi le groupe comprenant alkylène en 01-020,
cycloalkylène en
03-012, cycloalcénylène en 06-012, et arylène en 06-012, chaque groupe étant
éventuellement
substitué par 1, 2, 3, ou 4 groupements, identiques ou différents, choisis
parmi le groupe
comprenant un atome d'halogène, -OH, -CHO, nitro, -0O2R60, -N R92, alkyle en
Cl-06, alkoxy
en Cl-04, hydroxyalkyle en Cl-06, et aryle en 06-012; de préférence L2 est une
liaison
covalente simple, ou est choisi parmi le groupe comprenant alkylène en Cl-011,
cycloalkylène en 03-012, et arylène en 06-012, chaque groupe étant
éventuellement substitué
par 1, 2, 3, ou 4 groupements, identiques ou différents, choisis parmi le
groupe comprenant
un atome d'halogène, -OH, -CHO, -0O2R60, alkyle en Cl-06, et aryle en 06-012;
de
préférence L2 est une liaison covalente simple, ou est un alkylène en Cl-011,
ou un
cycloalkylène en 03-012; éventuellement substitué par 1, 2, ou 3 groupements,
identiques ou
différents, choisis parmi le groupe comprenant un atome d'halogène, -OH, -CHO,
-002R60
,
alkyle en Cl-06, et aryle en 06-012;
R6 est choisi parmi les groupes comprenant H ou alkyle en Cl-06
éventuellement substitué
par un ou plusieurs groupements (par exemple 1, 2, 3, ou 4), identiques ou
différents, choisis
parmi le groupe comprenant -OH, -CHO, -0-COR7, et alkyle en Cl-06; de
préférence R6 est
choisi parmi les groupes comprenant H ou alkyle en Cl-04 éventuellement
substitué par 1, 2
ou 3 groupements, identiques ou différents, choisis parmi le groupe comprenant
-OH, -CHO,
-0-COR7, et alkyle en Cl-04;
R7 est choisi parmi le groupe comprenant alkyle en Cl-024, alcényle en 02-020,
et aryle en
06-012, chaque groupe étant éventuellement substitué par un ou plusieurs
groupements,
identiques ou différents, choisis parmi le groupe comprenant -OH, époxy et -
000L1R5 ; de
préférence R7 est choisi parmi le groupe comprenant alkyle en 04-024, alcényle
en 04-020, et
aryle en 06-012, chaque groupe étant éventuellement substitué par 1, 2 ou 3
groupements
identiques ou différents, choisis parmi -OH, époxy, ou -000L1R5 ; de
préférence R7 est
choisi parmi le groupe comprenant alkyle en 06-024, et alcényle en 06-020,
chaque groupe
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
17
étant éventuellement substitué par 1, 2 ou 3 groupements identiques ou
différents, choisis
parmi -OH, époxy, ou -000L1R5 ; de préférence R7 est choisi parmi le groupe
comprenant
alkyle en C10-C24, et alcényle en C10-C20, chaque groupe étant éventuellement
substitué par
1, 2 ou 3 groupements identiques ou différents, choisis parmi -OH, époxy, ou -
000L' R5 ; de
préférence R7 est choisi parmi le groupe comprenant alkyle en C18-C24, et
alcényle en
C18-C20, chaque groupe étant éventuellement substitué par 1, 2 ou 3
groupements identiques
ou différents, choisis parmi -OH, époxy, ou -000L1R5 ;
R8 est choisi parmi le groupe H ou alkyle en Cl-06; de préférence R8 est
choisi parmi le
groupe H ou alkyle en Cl-04; de préférence R8 est choisi parmi le groupe H ou
alkyle en
C1-C2 ; et
chaque R9 identique ou différent est choisi parmi le groupe H, alkyle en 01-
06, ou aryle en
06-012, de préférence chaque R9 identique ou différent est choisi parmi le
groupe H ou alkyle
en Cl-04; de préférence chaque R9 identique ou différent est choisi parmi le
groupe H ou
alkyle en Cl-02.
Le terme alkyle en Cl-020 fait référence à un radical hydrocarboné saturé
linéaire ou
ramifié, comprenant de 1 à 20 atomes de carbone, tel que méthyle, éthyle,
propyle,
isopropyle, butyle, tert-butyle, isobutyle, pentyle, hexyle, heptyle, octyle,
nonyle, décyle,
undécyle, dodécyle, tridécyle, tétradécyle, pentadécyle, hexadécyle,
heptadécyle,
octadécyle, nonadécyle ou icosyle.
Le terme alcényle en Cl-020 fait référence à un radical hydrocarboné
linéaire ou ramifié,
comprenant une ou plusieurs double-liaisons, ayant de 2 à 20 atomes de
carbone. Ramifié
signifie qu'un ou plusieurs groupes alkyle inférieurs, tels que le méthyle,
l'éthyle ou le
propyle, sont liés à une chaîne alcényle linéaire. A titre d'exemple
d'alcényle en Cl-020 on
peut citer, le groupement éthényle, 1-propényle, 2-propényle, 1-butényle, 2-
butényle, 1-
pentényle, 2-pentényle, 3-méthy1-3-butényle, 1-hexényle, 2- hexènyle, 1-
heptényle, 2-
heptényle, 3-heptényle, 1-octényle, 4-octényle, 4-nonényle, 5-décényle, 5-
undécényle, 6-
dodécényle, tetradécényle, 9-hexadécènyle, 9-octadécènyle, 13-docosaènyle, 15-
tétracosaènyle, 9,12-octadécadiènyle, 9,12,15-octadécatriènyle, 6,9,12-
octadécatriènyle,
8, 11,14-eïcosatriènyle, 5,8,11, 14-éicosatétraènyle,
5,8, 11, 14,17-éicosapentaènyle,
4,7,10,13,16,19-docosahexaènyle.
Le terme cycloalkyle en 05-012 fait référence à un radical hydrocarboné
mono- ou
multicyclique saturé, ayant de 5 à 12 atomes de carbone. A titre d'exemple de
cycloalkyle
monocyclique, on peut citer par exemple le cyclopentyle, le cyclohexyle, le
cycloheptyle, le
cyclooctyle, le cyclodécyle, le cyclododécyle. A titre d'exemple de groupe
cycloalkyle
multicyclique, on peut citer notamment la 1-décaline, le norbornyle, ou
l'adamant-(1 ou
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
18
2-)yle.
Le terme cycloalcényle en 05-012 fait référence à un groupe dérivé d'un
groupe
cycloalkyle tel que défini ci- dessus, présentant une ou plusieurs doubles
liaisons. Il s'agit par
exemple du groupement cyclopentényle, cyclohéxényle, cyclopenta-1,3-diènyle,
cyclohéptényle, cyclooctényle, cycloocta-1,4-diényle, cyclodécényle, cyclodéca-
1,5-diényle,
Le terme alcynyle en 02-020 , fait référence à une chaîne hydrocarbonée
linéaire ou
ramifiée comprenant une ou plusieurs triples liaisons. Ramifié signifie qu'un
ou plusieurs
groupes alkyle inférieurs, tels que le méthyle, l'éthyle ou le propyle, sont
liés à une chaîne
alcynyle linéaire. Des exemples de groupes alcynyle sont notamment les groupes
éthynyle, 1
-propynyle, 1 -butynyle, 2-butynyle, etc.
Le terme aryle en 06-012 fait référence à un radical hydrocarboné
monocyclique ou
multicyclique aromatique, ayant 6 à 12 atomes de carbone, plus
préférentiellement 6 atomes
de carbone. Les groupes aryles incluent notamment les groupes phényle,
naphtyle et bi-
phényle.
Le terme C1_6alkylaryle en C6-C12 fait référence à un groupe aryle
substitué par au moins
un groupe alkyle en Cl-06, les groupes aryle et alkyle étant tel que définis
ci-dessus.
Le terme 06-C12arylalkyle en 01_6 OU aralkyle fait référence à un groupe
alkyle
substitué par au moins un groupe aryle en 06-012, les groupes aryle et alkyle
étant tel que
définis ci-dessus. Comme exemple de groupes aralkyle, on peut citer notamment
le benzyle,
le 2-phénéthyle et le naphtalèneméthyle.
Le terme alkoxy en Cl-04 fait référence à un groupe alky1-0- dans lequel
le terme alkyle
a la signification donnée ci-dessus. Des exemples de groupes alkoxy en Cl-04
sont les
groupes méthoxy, éthoxy, propoxy, butoxy.
Le terme 06-C12aryloxy fait référence à un groupe aryle-0- dans lequel le
terme aryle a la
signification donnée ci-dessus. Un exemple de groupe 06-C12aryloxy est le
phénoxy.
Le terme hétérocycloalkyle fait référence à des systèmes hydrocarbonés
mono-, bi- ou
poly-cycliques, saturés ou non, présentant sur le (ou les) cycle(s) au moins
un hétéroatome,
tel que l'azote, le soufre ou l'oxygène. Ils sont non aromatiques. A titre
d'hétérocycle, on peut
notamment citer le groupe pipéridine, pipérazine, pyrrolidine, pyrrolidinone,
morpholine,
phtalane, phtalide, thiazolidinedione, sulfolane, benzo[I,3]dioxolane,
benzo[I,4]dioxane,
[2,3]dihydrobenzofurane, quinazolinone, benzothiadiazinone, 1-méthyl-piperidin-
4-yle ou 1-
méthyl-piperidin-4-ylméthyle.
Le terme hétéroaryle fait référence à un ou plusieurs cycles insaturés
aromatiques
comprenant un ou plusieurs hétéroatomes identiques ou différents choisis parmi
N, 0 et S,
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
19
tels que les groupes pyridinyle, pyrimidinyle, furyle, thiènyle,
benzothiènyle, oxazolyle,
benzoxazolyle, isoxazolyle, thiazolyle, pyrolyle, pyrazolyle, imidazolyle,
triazolyle, tétrazolyle.
Le terme alkylène en Ci-C , fait référence à un groupe alkyle divalent
saturé, linéaire ou
ramifié. Des exemples de groupes alkylènes sont notamment les groupes
méthylène,
éthylène, 1-méthyléthylène, propylène, etc.
Le terme alcénylène en 02-012 fait référence à un groupe alcényle
divalent, le groupe
alcényle étant tel que défini ci-dessus.
Le terme cycloalkylène en 03-012 fait référence à un groupe cycloalkyle
divalent, le
groupe cycloalkyle étant tel que défini ci-dessus.
Le terme arylène en 06-012 fait référence à un groupe aryle divalent, le
groupe aryle
étant tel que défini précédemment.
Le terme hétérocycloalkylène fait référence à un groupe hétérocycloalkyle
divalent, le
groupe hétérocycloalkyle étant tel que défini précédemment.
Le terme hétéroarylène fait référence à un groupe hétéroarylène divalent,
le groupe
hétéroarylène étant tel que défini précédemment.
Le terme hydroxyalkyle désigne les groupes dans lesquels le groupe alkyle
est tel que
défini ci-dessus et dont au moins un atome de carbone est substitué par un
radical hydroxy
comme par exemple hydroxyméthyle, hydroxyéthyle, 2-hydroxy-butyle.
Le terme halogène ou atome d'halogène fait référence à un atome de
chlore, brome,
fluor ou iode.
Le terme oxo fait référence à un groupe =0.
Le terme cyano fait référence à un groupe ¨CEN.
Le terme époxy fait référence à un groupe ou
Par le terme "polymère", on entend une molécule de formule (1c) ou (Id),
R3 R4 R2 1
R60 R60 ï
0 0
R2 R4
R5-A P p
(1c) (Id)
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
dans laquelle p est répété un grand nombre de fois (jusqu'à plusieurs
milliers). Par exemple,
p est un indice entier compris entre 1 et 10 000, de préférence p est un
indice entier compris
entre 1 et 1000, par exemple p est un indice entier compris entre 1 et 100. De
préférence le
polymère du composé de formule (la) ou (lb) est un oligomère. Par "oligomère",
on entend
5 une molécule de formule (1c) ou (Id) dans laquelle p est répété moins de
20 fois (p indice
entier inférieur à 20).
Les définitions ci-dessus sont applicables à la description, à l'exemplarité
et aux
revendications de l'invention. Pour faciliter la compréhension, la
nomenclature des
groupements, des réactifs, des solvants ou des produits est la nomenclature
internationale
10 ou la nomenclature couramment utilisée par l'homme du métier.
Selon un mode de réalisation préféré, l'invention concerne un procédé de
synthèse des
composés de la famille représentée par la formule (la) ou (lb), un stéréo-
isomère, un
mélange de composés de cette famille, et/ou un oligomère et/ou un polymère de
ceux-ci,
dans lesquelles
15 R1 est H ou est choisi parmi le groupe comprenant alkyle en Cl-020,
alcényle en 02-020, et
aryle en 06-012, chaque groupe étant éventuellement substitué par 1, 2 ou 3
groupements,
identiques ou différents, choisis parmi le groupe comprenant -OH, -CHO, oxo,
cyano, -N R92,
époxy, alkoxy en Cl-04, alkyle en 01-06, aryle en 06-012, -000L1R5, -000R8, et
-0O2R80;
R2 est H ou est choisi parmi le groupe comprenant alkyle en 01-020, alcényle
en 02-020, aryle
20 en 06-012, et 06-C12arylalkyle en 01_6, chaque groupe étant
éventuellement substitué par 1, 2
ou 3 groupements, identiques ou différents, choisis parmi le groupe comprenant
-OH, -CHO,
époxy, oxo, cyano, -NR92, alkoxy en 01-04, alkyle en Cl-06, aryle en 06-012, -
OCOL1R8,
-000R8, et -002R60;
R3 est choisi parmi le groupe comprenant alkyle en Cl-020, alcényle en 02-020,
et aryle en
06-012, chaque groupe étant éventuellement substitué par 1, 2 ou 3
groupements, identiques
ou différents, choisis parmi le groupe comprenant -OH, -CHO, oxo, époxy,
alkoxy en Cl-04,
alkyle en Cl-06, aryle en 06-012, -000L1R8 et -002R60;
R4 est H, ou est choisi parmi le groupe comprenant alkyle en Cl-020, alcényle
en 02-020, et
aryle en 06-012, chaque groupe étant éventuellement substitué par 1, 2 ou 3
groupements,
identiques ou différents, choisis parmi le groupe comprenant -OH, -CHO, oxo,
époxy, alkoxy
en Cl-04, alkyle en Cl-06, aryle en 06-012, -000L1R8, et -002R8 ;
ou bien R1 et R3 peuvent former, avec les carbones auxquels ils sont liés, un
groupe choisi
parmi un cycloalkyle en 05-012 ou un cycloalcényle en 05-012, chaque groupe
étant
éventuellement substitué 1, 2, 3 ou 4 groupements, identiques ou différents,
choisis parmi le
groupe comprenant un -OH, oxo, époxy, -000L1R8, -000R8, -002R80, alkyle en Cl-
06, et
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
21
alcényle en 02-06;
R5 est choisi parmi le groupe comprenant Cl, F, 1, Br, -OH, -SH, -CHO, époxy,
cyano, nitro,
isocyanate, alkoxy en 01-04, alcényle en 02-012, alcynyle en 02-012,
hétérocycloalkyle,
-002R8, et -NR92 ;
R6 est H ou -00-Ll-R5 ;
12 est une liaison covalente simple, ou est choisi parmi le groupe comprenant
alkylène en
01-020, cycloalkylène en 03-012, cycloalcénylène en 05-012, et arylène en 06-
012, chaque
groupe étant éventuellement substitué par 1, 2, 3, ou 4 groupements,
identiques ou
différents, choisis parmi le groupe comprenant un atome d'halogène, -OH, oxo, -
CHO,
-000L1R5, -002R60, -NR92, alkyle en 01-06, alkoxy en 01-04, hydroxyalkyle en
01-06, et aryle
en 06-012;
R6 est choisi parmi les groupes comprenant H et alkyle en 01-04
éventuellement substitué
par 1, 2 ou 3 groupements, identiques ou différents, choisis parmi le groupe
comprenant
-OH, -CHO, -0-COR7, et alkyle en 01-04;
R7 est choisi parmi le groupe comprenant alkyle en 04-024, alcényle en 04-020,
et aryle en
06-012, chaque groupe étant éventuellement substitué par 1, 2 ou 3 groupements
identiques
ou différents, choisis parmi le groupe comprenant -OH, époxy et -000L1R5 ;
R8 est choisi parmi le groupe H ou alkyle en 01-04; et
chaque R9 identique ou différent est choisi parmi le groupe H ou alkyle en 01-
04.
Selon un mode de réalisation préféré, l'invention concerne un procédé de
synthèse des
composés de la famille représentée par la formule (la) ou (lb), un stéréo-
isomère, un
mélange de composés de cette famille, et/ou un oligomère et/ou un polymère de
ceux-ci,
dans lesquelles
R1 est H ou est choisi parmi le groupe comprenant alkyle en 01-020, et
alcényle en 02-020,
chaque groupe étant éventuellement substitué par 1, 2 ou 3 groupements,
identiques ou
différents, choisis parmi le groupe comprenant -OH, oxo, alkoxy en 01-02,
alkyle en 01-06,
-000L1R5, et -002R60;
R2 est H ou est choisi parmi le groupe comprenant alkyle en 01-020, et
alcényle en 02-020,
chaque groupe étant éventuellement substitué par 1, 2 ou 3 groupements,
identiques ou
différents, choisis parmi le groupe comprenant oxo, alkoxy en 01-02, alkyle en
01-06,
-000L1R5, et -002R60;
R3 est choisi parmi le groupe comprenant alkyle en 01-020, et alcényle en 02-
020, chaque
groupe étant éventuellement substitué par 1, 2 ou 3 groupements, identiques ou
différents,
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
22
choisis parmi le groupe comprenant -OH, oxo, alkoxy en Cl-02, alkyle en 01-06,
-000L1R5 et
-002R6 ;
R4 est H, ou est choisi parmi le groupe comprenant alkyle en 01-020, et
alcényle en 02-020,
chaque groupe étant éventuellement substitué par 1, 2 ou 3 groupements,
identiques ou
différents, choisis parmi le groupe comprenant oxo, alkoxy en Cl-02, alkyle en
Cl-06,
-000L1R5, et -002R60;
ou bien R1 et R3 peuvent former, avec les carbones auxquels ils sont liés, un
groupe choisi
parmi un cycloalkyle en 05-010 et un cycloalcényle en 05-010, chaque groupe
étant
éventuellement substitué 1, 2, ou 3 groupements, identiques ou différents,
choisis parmi le
groupe comprenant -OH, époxy, alkyle en 01-06, et alcényle en 02-06;
R5 est choisi parmi le groupe comprenant Cl, F, I, Br, -OH, -CHO, époxy, -SH,
cyano, et nitro,
de préférence -OH, -SH, époxy, cyano ou nitro, de préférence -OH, -SH, époxy
ou cyano;
R6 est H ou ¨00-Ll-R5 ;
L1 est une liaison covalente simple, ou est choisi parmi le groupe comprenant
alkylène en
01-011, cycloalkylène en 03-012, et arylène en 06-012, chaque groupe étant
éventuellement
substitué par 1, 2, 3, ou 4 groupements, identiques ou différents, choisis
parmi le groupe
comprenant un atome d'halogène, -OH, -CHO, -000L1R5, -002R69, alkyle en 01-06,
et aryle
en 06-012;
R69 est choisi parmi le groupe comprenant H et alkyle en Cl-04 éventuellement
substitué par
1, 2 ou 3 groupements, identiques ou différents, choisis parmi le groupe
comprenant -OH,
-CHO, -0-COR7, et alkyle en Cl-04;
R7 est choisi parmi le groupe comprenant alkyle en 06-024, et alcényle en 06-
020, chaque
groupe étant éventuellement substitué par 1, 2 ou 3 groupements, identiques ou
différents,
choisis parmi le groupe comprenant -OH, époxy et -000L1R5 ;
R8 est choisi parmi le groupe H ou alkyle en Cl-04; et
chaque R9 identique ou différent est choisi parmi le groupe H ou alkyle en Cl-
04.
L'invention porte donc sur un procédé de préparation de composés de formule
(la), (lb), (1c)
ou (Id), ou un mélange de ceux-ci, ledit procédé comprenant la réaction d'au
moins une
molécule insaturée de formule (II) avec de l'oxygène atmosphérique ou
moléculaire, en
présence d'au moins un aldéhyde de formule (III), et facultativement en
présence d'au moins
un catalyseur ou d'au moins un initiateur de radicaux. Selon un mode de
réalisation
particulier, la molécule insaturée de formule (II) peut être la même molécule
que l'aldéhyde
de formule (III).
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
23
Selon un mode de réalisation particulier, le procédé comprend la réaction
d'une molécule
insaturée de formule (II) avec de l'oxygène atmosphérique ou moléculaire, en
présence d'au
moins un aldéhyde de formule (III) et facultativement en présence d'au moins
un catalyseur
ou d'au moins un initiateur de radicaux ; dans lesquelles
R1 est H, ou est choisi parmi le groupe comprenant alkyle en Cl-020, alcényle
en 02-020, et
aryle en 06-012, chaque groupe étant éventuellement substitué par 1, 2, ou 3
groupements,
identiques ou différents, choisis parmi le groupe comprenant -OH, -CHO, oxo,
cyano, -NR92,
époxy, alkoxy en 01-04, -000L2R50, alkyle en 01-06, aryle en 06-012, -000R8,
et -002R60;
R2 est H ou -CHO ou est choisi parmi le groupe comprenant alkyle en 01-020,
alcényle en
02-020, et aryle en 06-012, chaque groupe étant éventuellement substitué par
1, 2, ou 3
groupements, identiques ou différents, choisis parmi le groupe comprenant -OH,
-CHO, oxo,
cyano, -NR92, époxy, alkoxy en 01-04, -000L2R50, alkyle en Cl-06, aryle en 06-
012, 000R8,
et -002R60;
R3 est choisi parmi le groupe comprenant époxy, alkyle en Cl-020, alcényle en
02-020, et
aryle en 06-012, chaque groupe étant éventuellement substitué par 1, 2 ou 3
groupements,
identiques ou différents, choisis parmi le groupe comprenant -OH, alkyle en Cl-
06, -CHO,
oxo, époxy, alkoxy en Cl-04, -000L2R50, aryle en 06-012, -000R8, et -002R60;
R4 est H ou -CHO, ou est choisi parmi le groupe comprenant alkyle en Cl-020,
alcényle en
02-020, et aryle en 06-012, chaque groupe étant éventuellement substitué par
1, 2 ou 3
groupements, identiques ou différents, choisis parmi le groupe comprenant -OH,
oxo, époxy,
alkoxy en Cl-04, alkyle en Cl-06, aryle en 06-012, -000L2R50, et -002R60;
ou bien R1 et R3 peuvent former, avec les carbones auxquels ils sont liés,
un groupe choisi
parmi un cycloalkyle en 05-012 ou un cycloalcényle en 05-012, chaque groupe
étant
éventuellement substitué par 1, 2, 3, ou 4 groupements, identiques ou
différents, choisis
parmi le groupe comprenant -OH, -CHO, oxo, époxy, -000L2R50, alkyle en Cl-06,
et alcényle
en 02-06;
R5 est choisi parmi le groupe comprenant Cl, F, I, Br, -OH, -CHO, époxy, -SH,
cyano, nitro,
isocyanate, alcényle en 02-012, alcynyle en 02-012, hétérocycloalkyle, -002R8,
et -NR92 ;
L2 est une liaison covalente simple, ou est choisi parmi le groupe comprenant
alkylène en
Cl-Cm, cycloalkylène en 03-012, cycloalcénylène en 05-012, et arylène en 06-
012, chaque
groupe étant éventuellement substitué par 1, 2, 3, ou 4 groupements,
identiques ou
différents, choisis parmi le groupe comprenant un atome d'halogène, -OH, -CHO,
nitro,
-002R60, -NR92, alkyle en Cl-06, alkoxy en Cl-04, hydroxyalkyle en Cl-06, et
aryle en 06-012;
R6 est choisi parmi les groupes comprenant H et alkyle en Cl-04
éventuellement substitué
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
24
par 1, 2 ou 3 groupements, identiques ou différents, choisis parmi le groupe
comprenant
-OH, -CHO, -0-COR7, et alkyle en Cl-04;
R7 est choisi parmi le groupe comprenant alkyle en 04-024, alcényle en 04-020,
et aryle en
06-012, chaque groupe étant éventuellement substitué par 1 2, ou 3
groupements, identiques
ou différents, choisis parmi le groupe comprenant -OH, époxy et -000L1R8 ;
R8 est choisi parmi le groupe H ou alkyle en Cl-04; et
chaque R9 identique ou différent est choisi parmi le groupe H ou alkyle en Cl-
04.
Selon un mode de réalisation préféré, le procédé comprend la réaction d'une
molécule
insaturée de formule (II) avec de l'oxygène atmosphérique ou moléculaire, en
présence d'au
moins un aldéhyde de formule (III) et facultativement en présence d'au moins
un catalyseur
ou d'au moins un initiateur de radicaux ; dans lesquelles
R19 est H, ou est choisi parmi le groupe comprenant alkyle en 01-020, et
alcényle en 02-020,
chaque groupe étant éventuellement substitué par 1, 2, ou 3 groupements,
identiques ou
différents, choisis parmi le groupe comprenant -OH, -CHO, oxo, -000L2R89,
alkoxy en Cl-02,
et alkyle en Cl-06;
R29 est H ou -CHO, ou est choisi parmi le groupe comprenant alkyle en Cl-020,
et alcényle
en 02-020, chaque groupe étant éventuellement substitué par 1, 2, ou 3
groupements,
identiques ou différents, choisis parmi le groupe comprenant -OH, oxo, -CHO, -
000L2R89,
alkoxy en Cl-02, et alkyle en Cl-06;
R39 est choisi parmi le groupe comprenant alkyle en Cl-020, et alcényle en 02-
020, chaque
groupe étant éventuellement substitué par 1, 2 ou 3 groupements, identiques ou
différents,
choisis parmi le groupe comprenant oxo, alkoxy en Cl-02, alkyle en Cl-06, -
CHO, -000L2R89
et -002R89 ;
Re est H ou -CHO, ou est choisi parmi le groupe comprenant alkyle en Cl-020,
et alcényle
en 02-020, chaque groupe étant éventuellement substitué par 1, 2 ou 3
groupements,
identiques ou différents, choisis parmi oxo alkoxy en Cl-02, alkyle en Cl-06, -
000L2R89, ou
-002R60;
ou bien R19 et R39 peuvent former, avec les carbones auxquels ils sont liés,
un groupe choisi
parmi un cycloalkyle en 05-010 ou un cycloalcényle en 05-010, chaque groupe
étant
éventuellement substitué par 1, 2, ou 3 groupements, identiques ou différents,
choisis parmi
le groupe comprenant -OH, -CHO, époxy, alkyle en Cl-06, et alcényle en 02-06;
R89 est choisi parmi le groupe comprenant Cl, F, I, Br, -OH, -CHO, époxy, -SH,
cyano, et
nitro,
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
L2 est une liaison covalente simple, ou est choisi parmi le groupe comprenant
alkylène en
Ci-Cii, cycloalkylène en C3-C12, et arylène en C6-C12, chaque groupe étant
éventuellement
substitué par 1, 2, 3, ou 4 groupements, identiques ou différents, choisis
parmi le groupe
comprenant un atome d'halogène, -OH, nitro, -CHO, -0O2R89, alkyle en Cl-06, et
aryle en
5 06-012;
R89 est choisi parmi les groupes comprenant H et alkyle en Cl-04
éventuellement substitué
par 1, 2 ou 3 groupements, identiques ou différents, choisis parmi le groupe
comprenant
-OH, -CHO, -0-COR7, et alkyle en Cl-04;
R7 est choisi parmi le groupe comprenant alkyle en 06-024, et alcényle en 06-
020, chaque
10 groupe étant éventuellement substitué par 1 ou 2 groupements, identiques
ou différents,
choisis parmi le groupe comprenant -OH, époxy et -000L1R8 ;
R8 est choisi parmi le groupe H ou alkyle en Cl-04; et
chaque R9 identique ou différent est choisi parmi le groupe H ou alkyle en Cl-
04.
Selon un mode de réalisation particulier, le procédé peut être réalisé à
pression
15 atmosphérique. Selon un autre mode de réalisation particulier, le
procédé peut être réalisé
sous pression avec ou sans débit constant d'oxygène ou d'air. Le débit
d'oxygène peut être
contrôlé, par exemple par un débitmètre. Avantageusement, le milieu
réactionnel est
maintenu à saturation en oxygène dissous.
Selon un mode de réalisation particulier, le procédé comprend la réaction d'au
moins une
20 molécule insaturée de formule (II) avec de l'oxygène atmosphérique ou
moléculaire, en
présence d'au moins un aldéhyde de formule (III).
Selon un autre mode de réalisation particulier, le procédé comprend la
réaction d'au moins
une molécule insaturée de formule (II) avec de l'oxygène atmosphérique ou
moléculaire, en
présence d'au moins un aldéhyde de formule (III), et en présence d'au moins un
catalyseur
25 ou en présence d'au moins un initiateur de radicaux tel que
l'azobisisobutyronitrile (AIBN),
l'azobiscyanocyclohexane (ACHN) ou l'acide azobis(4-cyanopentanoique) (ACVA).
Selon un
mode de réalisation préféré, la réaction est réalisée en présence d'un
catalyseur, de
préférence un catalyseur solide.
Selon ce mode de réalisation, le procédé est un processus de catalyse
hétérogène. Ainsi, le
catalyseur n'est pas consommé dans la réaction et ne se retrouve pas dissous
dans le milieu
réactionnel. En restant sous forme solide, il est facilement séparé du milieu
réactionnel sans
perte de catalyseur et sans pollution du milieu réactionnel par des espèces
dissoutes ou des
résidus de catalyseur. Le catalyseur solide peut être éliminé par simple
filtration ou alors
immobilisé dans un lit catalytique permettant dans les deux cas son recyclage.
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
26
De préférence, le catalyseur massique ou supporté est un catalyseur à base
d'un métal du
groupe 6 à 12 de la classification périodique des éléments et l'on peut citer,
préférentiellement, les catalyseurs à base de ruthénium, palladium, platine,
cobalt,
manganèse, nickel, cuivre, zinc ou fer, déposés par exemple sur un support
solide tel que
les alumines, les charbons actifs, les oxydes de zinc, de magnésium, de
titane, les silices,
les zéolithes ou des résines polymériques. Selon un mode de réalisation
particulier, le
catalyseur est choisi parmi le groupe comprenant les catalyseurs à base de
ruthénium,
palladium, platine, cobalt, manganèse, nickel, cuivre, zinc ou fer ou de
charbons actifs. Selon
un mode de réalisation préféré, le catalyseur est un catalyseur à base de
ruthénium, de
nickel ou de cobalt supporté, ou de charbon actif. De préférence, le
catalyseur est un
catalyseur à base de ruthénium, ou de cobalt supporté.
Selon un mode de réalisation préférée, le catalyseur est à base de ruthénium
supporté sur
de la silice préparé au départ du chlorure de ruthénium et d'une silice
colloïdale.
Selon un autre mode de réalisation préféré, le catalyseur est un catalyseur à
base de nickel
supporté, par exemple un catalyseur à base de nickel supporté sur du charbon
actif.
Le catalyseur peut être introduit dans la réaction à raison de 0 à 10% en
masse de la
quantité de molécule insaturée engagée, par exemple de 0,1 à 10%, de
préférence à raison
de 0,1 à 8%, de préférence à raison de 0,1 à 5%, avantageusement de 0,5 à 3%,
de
préférence à raison de 0,5 à 1%.
Selon un mode de réalisation particulier, le composé de formule (11) peut être
un alcène en
03-020, ou un cycloalcène en 05-012, chaque alcène ou cycloalcène étant
éventuellement
substitué par un ou plusieurs groupements, identiques ou différents choisis
parmi le groupe
comprenant un atome d'halogène, -CHO, -OH, cyano, oxo, époxy, -000R8, alkyle
en Cl-06,
alcényle en 02-06, aryle en 06-012, -000L2R50, et -002R6 ; chaque alkyle,
alcényle, ou aryle
étant éventuellement substitué par un ou plusieurs groupements, identiques ou
différents
choisis parmi le groupe comprenant un atome d'halogène, oxo, -CHO, -OH, alkyle
en Cl-06,
aryle en 06-012 -000L2R50, -000R8, et -002R60
.
Selon un mode de réalisation particulier, le composé de formule (11) est
choisi parmi le
groupe comprenant 1-pentène, 1-hexène, 1-heptène, 1-octène, 1-nonène, 1-
décène, 1-
undécène, 1-dodécène, 1-octadécène, 1-nonadécène, 1-tridécène, 1-tétradécène,
1-
hexadécene, 1-octadécène, 3-butène-1,2-diol, 2-butène-1,4-diol, 2-bromo-2-
butène, 1,4-
dichloro-2-butène, 2,3-diméthy1-2-butène, 2-chloro-2-butène, 3,4-époxy-1-
butène, 1,1-
diacetoxy-2-butène, 2,3-dibromo-2-butène-1,4-diol, 1-chloro-2-butène, 2-méthy1-
3-butèn-2-ol,
3-butèn-2-ol, 3-butèn-2-one, 3-butènenitrile, 2,3-diméthy1-1,3-butadiène, 2-
pentène, 2,4,4-
triméthy1-2-pentène, 2-méthy1-2-pentène, 3-éthy1-2-pentène, 5-o-tolyI-2-
pentène, 4-méthy1-2-
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
27
pentène, 1-pentèn-3-ol, 3-méthy1-3-pentèn-2-one, 4-méthy1-3-pentèn-2-one, 2-
hexène, 1,2-
époxy-5-hexène, 3,4-bis(4-hydroxyphény1)-3-hexène,
5-hexèn-2-one, 3-hexèn-1-01,
cyclohexène, 3-cyclohexène-1-carboxaldéhyde, 3-cyclohexène-1-méthanol, 4-viny1-
1-
cyclohexène, cyclohexène-1-carbonitrile, 1-cyclohexenylacétonitrile, p-mentha-
1,8-diène
(limonène), p-mentha-1,8-diène-7-ol, 1,4-cyclohexadiène, 1-isopropy1-4-méthy1-
1,3-
cyclohexadiène (terpinène), p-benzoquinone, 6-méthy1-5-heptèn-2-one,
bicyclo[2.2.1]hept-2-
ène (norbornène), (1r,5r)-2,6,6-triméthylbicyclo[3.1.1]hept-2-ène (pinène), 4-
octène, 1,7-
octadiène, acétate de 1-octèn-3-yle, cyclooctène, cyclooctadiène, 4-nonène, 10-
undécèn-1-
01, 7-tétradécene, 1,7-hexadécadiène, 1-amino-9-octadécène (oléylamine),
acrylate d'éthyle,
méthacrylate d'éthyle, isoprène, myrcène, styrène, a-méthylstyrène, acétate de
vinyle. Par
exemple, le composé de formule (Il) est choisi parmi le groupe comprenant 1-
octène, 3-
butènenitrile, 2,3-diméthy1-1,3-butadiène, 2-hexène, 3-hexèn-1-ol,
cyclohexène, 3-
cyclohexène-1-carboxaldéhyde, 1-cyclohexenylacétonitrile, p-mentha-1,8-diène
(limonène),
1-isopropy1-4-méthy1-1,3-cyclohexadiène (terpinène),
6-méthy1-5-heptèn-2-one,
bicyclo[2.2.1]hept-2-ène
(norbornène), (1r,50-2,6,6-triméthylbicyclo[3. 1.1 ]hept-2-ène
(pinène), 4-octène, cyclooctène, cyclooctadiène, 4-nonène, acrylate d'éthyle,
méthacrylate
d'éthyle, isoprène, myrcène, styrène, a-méthylstyrène. Par exemple, le composé
de formule
(Il) est choisi parmi le groupe comprenant 1-octène, 2-hexène, cyclohexène, 3-
cyclohexène-
1-carboxaldéhyde, 1-cyclohexenylacétonitrile, p-mentha-1,8-diène (limonène), 6-
méthy1-5-
heptèn-2-one, bicyclo[2.2.1]hept-2-ène (norbornène),
(1r,50-2,6,6-
triméthylbicyclo[3.1.1]hept-2-ène (pinène), 4-octène, cyclooctène,
cyclooctadiène, myrcène,
styrène, et a-méthylstyrène. Par exemple, le composé de formule (Il) est
choisi parmi le
groupe comprenant cyclohexène, 4-octène, cyclooctène, cyclooctadiène, myrcène,
styrène.
Selon un mode de réalisation particulier, le composé de formule (Il) est un
corps gras
insaturé, de préférence de formule R10CH=CH-(CH2)õ-CO2R6 dans laquelle u est
un indice
entier compris entre 2 et 11 ; de préférence u est choisi parmi 2, 3, 4, 5, 6,
7, 8, 9, ou 10, et
R1 et R6 ont la même signification que ci-dessus.
Le terme corps gras insaturé est utilisé de manière générique et il
désignera aussi bien
les acides gras insaturés à proprement parler, seuls ou en mélange avec des
acides gras
saturés, que leurs dérivés, c'est-à-dire leur forme ester alkylique en Cl-06,
ou glycérique tels
que mono-, di- ou triglycéride, ou glycolique et/ou leurs mélanges. La notion
d' acide gras
insaturé au sens de la présente description inclut en particulier les
composés insaturés
présents dans les huiles végétales et animales et les esters des acides gras
contenus dans
ces huiles ainsi que les acides gras (acides carboxyliques non estérifiés)
correspondants.
Comme exemples d'acides gras insaturés pouvant être utilisés dans la présente
invention,
on peut citer les acides gras insaturés présentant une seule double liaison
tel que les acides
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
28
lindérique, myristoléique, palmitoléique, oléique, pétrosélénique, doeglique,
gadoléique,
érucique ; les acides gras insaturés présentant deux doubles liaisons tels que
l'acide
linoléique ; les acides gras insaturés présentant 3 doubles liaisons tels que
l'acide linolénique
les acides gras insaturés présentant plus de 4 doubles liaisons tels que les
acides isanique,
stéarodonique, arachidonique, chypanodonique ; les acides gras insaturés
porteurs de
groupe hydroxyle tel que l'acide ricinoléique, leur ester alkylique en Cl-06,
ou leur forme
mono-, di- ou triglycéride, ou la combinaison de ceux-ci. Selon un mode de
réalisation
particulier, les acides gras insaturés sont choisi parmi le groupe comprenant
l'acide
undécylènique (3.9 undécylènique), l'acide lauroléique (3.9 dodécénoïque),
l'acide
myristoléique (3.9 tetradécénoïque), l'acide palmitoléique (3.9
héxacédécénoïque), l'acide
pétrosél inique (3.6 octadécénoïque), l'acide oléique (3.9c octadécénoïque),
l'acide élaïdique
(491 octadécénoïque), l'acide vaccénique (3.11t octadécénoïque), l'acide
ricinoléique (0H12,
491 octadécénoïque), l'acide linoléique (49C, 412c octadécadiénoïque), l'acide
linolénique
(A9c, 3,12c, 3,15c octadécatriénoïque), l'acide gondoïque (3.11 eicosénoïque),
l'acide érucique
(413 docosénoïque), l'acide vernolique (12,13-époxy-9-cis-octadécènoïque),
l'acide
coronorique (9,10-époxy-12-cis-octadécènoïque), l'acide alchornoïque (14,15-
époxy-11-cis-
éicosandique) leur ester alkylique en Cl-06, ou leur forme mono-, di- ou
triglycéride, ou la
combinaison de ceux-ci. Selon un mode de réalisation particulier, les acides
gras insaturés
sont choisi parmi le groupe comprenant l'acide undécylènique (3.9
undécylènique), l'acide
lauroléique (3.9 dodécénoïque), l'acide myristoléique (3.9 tetradécénoïque),
l'acide
palmitoléique (3.9 héxacédécénoïque), l'acide oléique (3.9c octadécénoïque),
l'acide élaïdique
(3.9t octadécénoïque), l'acide vaccénique (3.11t octadécénoïque), l'acide
ricinoléique (0H12,
3.9t octadécénoïque), l'acide linoléique (3.9c, 3.12c octadécadiénoïque),
l'acide linolénique
(A9c, 3,12c, 3,15c octadécatriénoïque), l'acide érucique (3.13 docosénoïque),
l'acide vernolique
(12,13-époxy-9-cis-octadécènoïque), leur ester alkylique en Cl-06, ou leur
forme mono-, di-
ou triglycéride, ou la combinaison de ceux-ci. Selon un mode de réalisation
particulier, les
acides gras insaturés sont choisis parmi le groupe comprenant l'acide
lauroléique (3.9
dodécénoïque), l'acide palmitoléique (3.9 héxacédécénoïque), l'acide oléique
(3.9c
octadécénoïque), l'acide ricinoléique (0H12, 3.9t octadécénoïque), l'acide
linoléique (3.9c,
3.12c octadécadiénoïque), l'acide linolénique (3.9c, 3,12c, 3,15c
octadécatriénoïque), leur ester
alkylique en Cl-06, ou leur forme mono-, di- ou triglycéride, ou la
combinaison de ceux-ci.
Selon un mode de réalisation particulier, les acides gras insaturés sont
choisis parmi le
groupe comprenant l'acide oléique (3.9c octadécénoïque), l'acide linoléique
(3.9c, 3,12c
octadécadiénoïque), l'acide linolénique (3.9c, Al 2c, 3,15c
octadécatriénoïque), leur ester
CA 02813286 2013-03-28
WO 2012/055946
PCT/EP2011/068824
29
alkylique en Cl-06, ou leur forme mono-, di- ou triglycéride, ou la
combinaison de ceux-ci.
A titres d'exemples de sources d'origine végétale, on peut mentionner, entre
autres, les
huiles de colza, tournesol, arachide, olive, noix, maïs, soja, lin, chanvre,
pépins de raisin,
coprah, palme, graines de coton, babassu, jojoba, sésame, ricin, coriandre,
carthame, tung.
II est également possible de partir des esters correspondants auxdits acides,
en particulier
les esters méthylique, éthylique et propylique et l'on peut citer plus
particulièrement les
produits d'alcoolyse, plus précisément de méthanolyse, des huiles notamment.
Selon un mode de réalisation particulier, l'aldéhyde de formule (111) est
choisi parmi le groupe
comprenant le formaldéhyde, l'acétaldéhyde, le propanal, le butyraldéhyde, le
valéraldéhyde,
l'hexanal, l'heptanaldéhyde, l'octanal, le nonanaldéhyde, le décanal,
l'undécanaldéhyde, le
laurinaldéhyde, le tridécanaldéhyde, l'isobutyraldéhyde,
l'isovaléraldéhyde, 2-
méthylbutyraldéhyde, le pivalaldéhyde, le 2- éthylbutaraldéhyde, le 2-
éthylhexanaldéhyde,
l'isodécanaldéhyde, l'acroléine, le crotonaldéhyde, le trans-2-hexèn-1-al, le
trans,trans-2,4-
hexadièn-1-al, le cis-4-heptènal, le trans-2-nonèn-1-al, le cis-4-décènal, le
citronellal,
l'hydroxycitronellal, le 1-cyclohexène-1-carboxaldéhyde, le 3-cyclohexène-1-
carboxaldéhyde,
le benzaldéhyde, le 3-hydroxybenzaldéhyde, le 4-hydroxybenzaldéhyde, le 4-
méthy1-2-
phény1-2-pentènal, l'aldéhyde para-tertiarybutyl-alpha-méthyl hydrocinnamique,
l'aldéhyde
amyl cinnamique, le glyoxal, le glutaraldéhyde, le furfuraldéhyde, le 3-
(méthylthio)propionaldéhyde, le 2-éthylacroléine, le 3-méthylcrotonaldéhyde,
le 2-méthy1-2-
butènal, le 4-oxobutanoate de méthyle, le cinnamaldéhyde, le 3-
diméthylaminoacroléine, le
cyclopentanecarboxaldéhyde, le 2,3,4,5,6-pentafluorobenzaldéhyde,
4-bromo-2,6-
difluorobenzaldéhyde, le 3,5-dibromobenzaldéhyde, le 3,5-dibromo-4-
hydroxybenzaldéhyde,
le 2,6-dinitrobenzaldéhyde, le 4-chlorobenzaldéhyde, le 2-chloro-4-
hydroxybenzaldéhyde, le
4-fluorobenzaldéhyde, le 5-fluorosalicylaldéhyde, le 4-nitrobenzaldéhyde, le 4-
hydroxy-3-
nitrobenzaldéhyde, le 3,5-dihydroxybenzaldéhyde, le 2,4,6-
trihydroxybenzaldéhyde, le 2-
aminobenzaldéhyde, le 2,4-heptadiènal, le 2,2-
diméthy1-4-pentènal, le 2-
cyanobenzaldéhyde, l'isophtalaldéhyde, le téréphtalaldéhyde, l'acide 4-
formylbenzoique,
l'acide 5-formylsalicylique, le o,m,p-tolualdehyde, le phénylacétaldéhyde, le
2,4-dihydroxy-6-
méthylbenzaldéhyde, le 3-vinylbenzaldéhyde, l'hydrocinnamaldéhyde, le 4-
hydroxy-3,5-
diméthylbenzaldéhyde, le mésitaldéhyde, le 2,4,6-triméthoxybenzaldéhyde, le 1-
naphtaldéhyde, le biphény1-4-carboxaldéhyde, le 3-phénoxybenzaldéhyde, le 4-(4-
formylphénoxy)benzaldéhyde, le diphénylacétaldéhyde, le 9-
anthracènecarboxaldéhyde, le
9-phénanthrènecarboxaldéhyde, le 5-(hydroxyméthyl)furfural (HM F), et le
tris(4-
formylphényl)amine. Par exemple, l'aldéhyde de formule (111) est choisi parmi
le groupe
comprenant l'acétaldéhyde, le propanal, le butyraldéhyde, le valéraldéhyde,
l'hexanal,
l'heptanaldéhyde, l'octanal, le nonanaldéhyde, le décanal, l'undécanaldéhyde,
le
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
laurinaldéhyde, le tridécanaldéhyde, l'isobutyraldéhyde,
l'isovaléraldéhyde, 2-
méthylbutyraldéhyde, le pivalaldéhyde, le 2-éthylbutaraldéhyde, le 2-
éthylhexanaldéhyde,
l'isodécanaldéhyde, l'acroléine, le crotonaldéhyde, le trans-2-hexèn-1-al, le
trans,trans-2,4-
hexadièn-1-al, le cis-4-heptènal, le trans-2-nonèn-1-al, le cis-4-décènal, le
citronellal,
5 l'hydroxycitronellal, le 1-cyclohexène-1-carboxaldéhyde, le 3-cyclohexène-
1-carboxaldéhyde,
le benzaldéhyde, le 3-hydroxybenzaldéhyde, le 4-hydroxybenzaldéhyde, le 4-
méthy1-2-
phény1-2-pentènal, le glutaraldéhyde, le furfuraldéhyde, le 2-éthylacroléine,
le 3-
méthylcrotonaldéhyde, le 2-méthy1-2-butenal, le cinnamaldéhyde, le 2,3,4,5,6-
pentafluorobenzaldéhyde, 4-bromo-2,6-difluorobenzaldéhyde, le 3,5-
dibromobenzaldéhyde,
10 le 3,5-dibromo-4-hydroxybenzaldéhyde, le 2,6-dinitrobenzaldéhyde, le 4-
chlorobenzaldéhyde, le 2-chloro-4-hydroxybenzaldéhyde, le 4-
fiuorobenzaldéhyde, le 5-
fluorosalicylaldéhyde, le 4-nitrobenzaldéhyde, le 4-hydroxy-3-
nitrobenzaldéhyde, le 3,5-
dihydroxybenzaldéhyde, le 2,4,6-trihydroxybenzaldéhyde, le 2-
aminobenzaldéhyde, le 1-
cyclohexène-1-carboxaldéhyde, le 2-cyanobenzaldéhyde, le 4-formylbenzonitrile,
le
15 téréphtalaldéhyde, l'acide 4-formylbenzoique, le 2,4-dihydroxy-6-
méthylbenzaldéhyde, le 3-
vinylbenzaldéhyde, le 1-naphtaldéhyde, et le 5-(hydroxyméthyl)furfural (HMF).
Selon un
mode de réalisation préféré, l'aldéhyde de formule (111) est choisi parmi le
groupe
comprenant l'hexanal, le décanal, le citronellal, l'hydroxycitronellal, le 3-
cyclohexène-1-
carboxaldéhyde, le benzaldéhyde, le 3-hydroxybenzaldéhyde, le 4-
hydroxybenzaldéhyde, le
20 furfuraldéhyde, le cinnamaldéhyde, le 3,5-dibromo-4-hydroxybenzaldéhyde, le
4-
chlorobenzaldéhyde, le 2-chloro-4-hydroxybenzaldéhyde, le 4-
fiuorobenzaldéhyde, le 5-
fluorosalicylaldéhyde, le 4-nitrobenzaldéhyde, le 4-hydroxy-3-
nitrobenzaldéhyde, le 3,5-
dihydroxybenzaldéhyde, le 2,4,6-trihydroxybenzaldéhyde, le 2-
aminobenzaldéhyde, le 1-
cyclohexène-1-carboxaldéhyde, le téréphtalaldéhyde, l'acide 4-formylbenzoique,
le 3-
25 vinylbenzaldéhyde, le 1-naphtaldéhyde, et le 5-(hydroxyméthyl)furfural
(HMF). Par exemple,
l'aldéhyde de formule (111) est choisi parmi le groupe comprenant l'hexanal,
le décanal, le
citronellal, l'hydroxycitronellal, le 3-cyclohexène-1-carboxaldehyde, le
benzaldéhyde, le 4-
hydroxybenzaldéhyde, le cinnamaldéhyde, le 4-chlorobenzaldéhyde, le
téréphtalaldéhyde,
l'acide 4-formylbenzoique, et le 5-(hydroxyméthyl)furfural (HMF). Par exemple,
l'aldéhyde de
30 formule (111) est choisi parmi le groupe comprenant l'hexanal, le décanal,
le citronellal,
l'hydroxycitronellal, le 3-cyclohexène-1-carboxaldéhyde, le téréphtalaldéhyde,
et le
benzaldéhyde.
Selon un mode de réalisation particulier, le composé de formule (111) est un
aldéhyde de
formule R50-(CR12R11)n-CHO, dans laquelle chaque R12, identique ou différent,
est choisi
parmi H ou alkyle en Cl-06, chaque R11, identique ou différent est choisi
parmi H, un atome
d'halogène, -CHO, -OH, ou alkyle en Cl-06, aryle en 06-012, C6-C12arylalkyle
en C1-6,
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
31
C1_6alkylaryle en 06-012, n est un indice entier compris entre 1 et 20, et R5
a la même
signification que donnée ci-dessus. Selon un mode de réalisation particulier,
n est choisi
parmi 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, ou
20. Selon un mode de
réalisation particulier, R12, identique ou différent, est choisi parmi H ou
alkyle en Cl-04,
chaque R11, identique ou différent est choisi parmi H ou alkyle en Cl-04,
aryle en 06-012,
Ci_elkylaryle en 06-012, Selon un mode de réalisation particulier, R5 est
choisi parmi le
groupe comprenant Cl, F, I, Br, -OH, -SH, cyano, nitro, isocyanate, alkoxy en
Cl-04, alcényle
en 02-020, alcynyle en 02-020, -002R8, époxy, ou -NR92. Par exemple, R5 est
choisi parmi le
groupe comprenant Cl, F, I, Br, -OH, -SH, cyano, ou nitro, de préférence -OH, -
SH, cyano ou
nitro, de préférence -OH, -SH ou cyano.
Selon un mode de réalisation particulier, l'aldéhyde de formule (III) est
utilisé en quantité
équimolaire, en défaut ou en excès par rapport au composé de formule (II).
Selon un mode de réalisation particulier, le composé de formule (la) ou (lb)
est préparé in
situ (procédé de synthèse monotope plus connu sous sa désignation anglaise
one-pot
réaction).
Selon un mode de réalisation particulier, la réaction implique deux étapes
successives
comprenant : l'époxydation du composé de formule (II) en présence d'oxygène
moléculaire
ou atmosphérique et d'au moins un aldéhyde de formule (III) et facultativement
en présence
d'au moins un catalyseur ; et l'ouverture de l'époxyde (cycle oxirane),
facultativement en
présence d'au moins un catalyseur qui peut être le même ou différent de celui
de l'étape
d'époxydation. Le procédé permet la synthèse de composés multifonctionnels en
une seule
étape par les réactions d'époxydation et d'acylation consécutives de molécules
insaturés.
Une des originalités de l'invention réside dans l'utilisation d'un aldéhyde
qui augmente
considérablement l'efficacité de la première étape de la réaction et qui,
ensuite, est utilisé
comme agent d'ouverture du cycle oxirane, l'aldéhyde étant transformé en acide
lors de la
première étape, tel qu'illustré au schéma 1. Une des originalités de
l'invention réside aussi
dans le fait que l'époxyde et l'acide ne sont que des intermédiaires de
réaction. Ils sont
générés in situ lors de la réaction. Une autre originalité réside en ce que
pendant
l'époxydation, la réaction d'ouverture à déjà lieu.
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
32
R20 R30 0 R20 R30 0
\ / Il\ / Il
C=C + 1:16, ,C 02 / cata> C=C + 1:16 -...., C
OH
/ \ - / \ 2,- -,,, õ,..-
L 0
Rio R4o L2 H Rio R4o
R2o R30 0 0
\ / H 0
),\ Il
C=C 1:150 r. (-114 021 cata R-I ,R3
/ \ + ====,.... L2,,,,,....a..........= = = -11,... ?/- +
Rio R4o
R2 R4
0 OR6 R, 3 R2 OR6
Il I I I I
R1 /O\ ,R3 1:16, C, R1¨C¨C¨R4 R1¨C¨C¨R4
CC
I \ +L1 -OH ¨ 1"-- ¨11" I I + I 1
R2 0 L1
L1 3
0 R
R2 R4 -...,....õ,--- -...R5 õ,-
"........./
FP
0 0
Schéma 1 mécanisme de la réaction one pot d'une molécule insaturée en
présence d'un
aldéhyde selon un mode de réalisation particulier de l'invention.
Ainsi, l'agent d'ouverture est généré in situ par transformation de l'aldéhyde
tout d'abord en
peracide, celui-ci pouvant soit régénérer le catalyseur soit réagir avec
l'insaturation du
composé (Il) pour être transformé en acide. Lors de la deuxième étape,
l'ouverture de
l'époxyde, la fonction acide permet l'ouverture et le greffage de la molécule
sur la molécule
de formule (Il) époxydée, par la création d'un lien ester et d'une fonction
alcool vicinale, la
fonction en bout de chaîne de l'ester représentant un nouveau centre
réactionnel (R5). Selon
un mode de réalisation particulier, l'hydroxyle vicinal peut aussi réagir
produisant ainsi un
composé de formule (la) et/ou (lb) dans laquelle R6 est -CO-L1R5.
Selon un mode de réalisation particulier, l'étape d'époxydation est réalisée à
une
température comprise entre 0 et 200 C, de préférence entre 20 et 150 C, de
préférence
entre 40 et 100 C, de préférence entre 50 et 80 C.
Selon un mode de réalisation particulier, l'étape d'ouverture de l'époxyde est
réalisée à une
température comprise entre 0 et 300 C, de préférence entre 30 et 300 C, de
préférence
entre 30 et 250 C, de préférence entre 30 et 200 C, de préférence entre 30 et
170 C.
Selon un mode de réalisation particulier, dans le cas d'une réaction monotope,
l'étape
d'époxydation et l'étape d'ouverture de l'époxyde sont réalisées à la même
température.
De préférence, l'étape d'ouverture est réalisée en présence d'azote. La
présence d'azote
permet de minimiser ou d'éviter les réactions secondaires comme par exemple
l'oxydation
lipidique dans le cas de l'utilisation de triglycérides ou de leurs dérivés
(autoxydation, photo-
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
33
oxydation).
Selon un mode de réalisation particulier, le présent procédé est réalisé en
l'absence de
solvant. Avantageusement, le procédé concerne une réaction one pot de
composés de
formule (II), utilisant l'oxygène moléculaire ou atmosphérique comme agent
d'oxydation en
présence d'un catalyseur solide, d'un aldéhyde et en l'absence d'un solvant.
Avantageusement, le procédé concerne une réaction one pot de corps gras
insaturés,
utilisant l'oxygène moléculaire ou atmosphérique comme agent d'oxydation en
présence d'un
catalyseur solide, d'un aldéhyde et en l'absence d'un solvant.
Selon un mode de réalisation particulier, le catalyseur solide est immobilisé
dans un
réacteur, le composé de formule (II) et l'aldéhyde de formule (III) sont
acheminés dans ce
dernier puis l'air ou l'oxygène moléculaire y est introduit soit par bullage à
pression
atmosphérique, soit sous pression. Selon un mode de réalisation particulier,
le milieu est
porté à la température de réaction de préférence entre 0 et 200 C, de
préférence entre 20 et
150 C, de préférence entre 40 et 100 C, de préférence entre 50 et 80 C
Des prélèvements peuvent être effectués régulièrement afin de mesurer
l'évolution de la
réaction d'époxydation. Lorsque celle-ci est complète, l'air peut être
remplacé par un gaz
inerte, typiquement l'azote, et le milieu peut être porté à plus haute
température de
préférence entre 30 et 200 C afin de provoquer la réaction d'ouverture de
l'époxyde par
l'acide généré in situ. On peut éventuellement ajouter catalyseur à ce stade
pour catalyser la
réaction d'ouverture. Ce catalyseur peut être solide tel qu'une zéolithe, une
hydrotalcite, un
charbon actif, une silice fonctionnalisée, ou une résine polymérique telle que
les résines
polymères basiques et/ou acide comme celles qui sont commercialisées sous la
dénomination Amberlyst ou Amberlite , ou une combinaison de ceux-ci. Ce
catalyseur
peut être homogène tel qu'une base minérale (KOH, NaOH), une amine primaire,
secondaire
ou tertiaire (hexylamine, dihexylamine, trihexylamine) ou une combinaison de
ceux-ci.
Une fois la réaction terminée, le milieu peut être ramené à la température
ambiante et retiré
du réacteur qui peut à nouveau accueillir les réactifs sans traitement
particulier, le catalyseur
étant réutilisable sans réactivation.
Selon un mode de réalisation particulier, par exemple pour une exploitation
industrielle, le
procédé est réalisé de façon continue ou bien dans deux ou plusieurs réacteurs
séparés.
La présente invention concerne aussi l'utilisation d'un procédé tel que décrit
ci-dessus pour
la préparation de polyesters polyhydroxylés.
La présente invention concerne aussi les composés de formule (la), (lb), (1c)
ou (Id)
susceptibles d'être obtenus par le procédé selon l'invention, et leur
utilisation par exemple
dans la préparation de polymères ou de biopolymères, en particulier de
polyuréthanes, de
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
34
polyesters polyhydroxylés, de bioplastiques, de tensio-actifs, de plastifiants
ou de lubrifiants.
Selon un mode de réalisation préféré, l'invention concerne aussi les composés
de formule
(la), (lb), (1c) ou (Id) directement obtenus par le procédé selon l'invention,
et leur utilisation
par exemple dans la préparation de polymères ou de biopolymères, en
particulier de
polyuréthanes, de polyesters polyhydroxylés, de bioplastiques, de tensio-
actifs, de
plastifiants ou de lubrifiants. De préférence, l'invention concerne
l'utilisation d'un composé de
formule (la) ou (lb) directement obtenu selon le procédé selon l'invention,
comme monomère
pour la préparation de polyuréthane.
L'invention concerne aussi un composé de formule (le) ou (If), un stéréo-
isomère de celui-ci,
ou un mélange de ceux-ci,
1 7 1 8
R 16 R 16
0R1 8
0 /\ R1 7
0R1 9 0 R1 9
(le)
dans lesquelles :
R16 est H ou est choisi parmi le groupe comprenant -00-(CR21R22)q_R23, _CO-
aryle en C6-C12,
et -CO-cycloalcényle en C5-C12, chaque groupe étant éventuellement substitué
par un ou
plusieurs groupements, identiques ou différents, choisis parmi le groupe
comprenant un
atome d'halogène, -OH, -000R19, -0O2R24, et alkyle en Cl-06; de préférence R16
est H ou
est choisi parmi le groupe comprenant -00-(0R21R22)q_R23, _CO-aryle en 06-010,
et
-CO-cycloalcényle en 05-010, chaque groupe étant éventuellement substitué par
un ou
plusieurs groupements, identiques ou différents, choisis parmi le groupe
comprenant un
atome d'halogène, -OH, -000R19, -0O2R24, et alkyle en Cl-06; de préférence R16
est H ou
est choisi parmi le groupe comprenant -00-(CR21R22)q_R23, _CO-aryle en 06, et
-CO-cycloalcényle en 05-08, chaque groupe étant éventuellement substitué par
un ou
plusieurs groupements, identiques ou différents, choisis parmi le groupe
comprenant un
atome d'halogène, -OH, -000R19, -002R24, et alkyle en Cl-04;
R17 est choisi parmi le groupe contenant un alkyle en 02-020 et un alcényle en
02-020,
chaque groupe étant éventuellement substitué par un ou plusieurs groupements,
identiques
ou différents, choisis parmi un alkyle en 01-06, un aryle en 06, -0R16, OU -
0O2R24 ; de
préférence R17 est choisi parmi le groupe comprenant un alkyle en 02-012 et un
alcényle en
02-020, chaque groupe étant éventuellement substitué par 1, 2, 3 ou 4
groupements,
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
identiques ou différents, choisis parmi un alkyle en Cl-06, un aryle en 06, -
0R16, OU -002R24;
de préférence R17 est choisi parmi le groupe comprenant un alkyle en 02-012 et
un alcényle
en 02-020, chaque groupe étant éventuellement substitué par 1, 2, 3 ou 4
groupements,
identiques ou différents, choisis parmi un alkyle en 01-06, -0R16, ou -002R24;
de préférence
5 R17 est un alkyle en 02-010 éventuellement substitué par 1, 2, ou 3
groupements, identiques
ou différents, choisis parmi un alkyle en 01-04, ou -002R24;
R18 est H ou est choisi parmi le groupe comprenant un alkyle en 02-020 et un
alcényle en
02-020, chaque groupe étant éventuellement substitué par un ou plusieurs
groupements,
identiques ou différents, choisis parmi un alkyle en 01-06, un aryle en 06, -
0R16, OU -002R24;
10 de préférence R18 est H ou est choisi parmi le groupe comprenant un
alkyle en 02-012 et un
alcényle en 02-020, chaque groupe étant éventuellement substitué par 1, 2, 3
ou 4
groupements, identiques ou différents, choisis parmi un alkyle en Cl-06, un
aryle en 06,
-0R16, OU -002R24; de préférence R18 est H ou est choisi parmi le groupe
comprenant un
alkyle en 02-012 et un alcényle en 02-020, chaque groupe étant éventuellement
substitué par
15 1, 2, 3 ou 4 groupements, identiques ou différents, choisis parmi un
alkyle en Cl-06, -0R16,
ou -002R24; de préférence R18 est H ou un alkyle en 02-010 éventuellement
substitué par 1,
2, ou 3 groupements, identiques ou différents, choisis parmi un alkyle en Cl-
04, ou -002R24;
ou bien R17 et R18 peuvent former, avec les carbones auxquels ils sont liés,
un groupe choisi
parmi un cycloalkyle en 05-012 ou un cycloalcényle en 05-012, chaque groupe
étant
20 éventuellement substitué par un ou plusieurs groupements, identiques ou
différents, choisis
parmi le groupe comprenant un atome d'halogène, -0R16, -000R19, -002R24, et
alkyle en
Cl-06; de préférence ou bien R17 et R18 peuvent former, avec les carbones
auxquels ils sont
liés, un groupe choisi parmi un cycloalkyle en 05-010 ou un cycloalcényle en
05-010, chaque
groupe étant éventuellement substitué par 1, 2, 3 ou 4 groupements, identiques
ou
25 différents, choisis parmi le groupe comprenant un atome d'halogène, -0R16, -
000R19,
-002R24, et alkyle en Cl-06; de préférence ou bien R17 et R18 peuvent former,
avec les
carbones auxquels ils sont liés, un groupe choisi parmi un cycloalkyle en 05-
08 ou un
cycloalcényle en 05-08, chaque groupe étant éventuellement substitué par 1, 2,
ou 3
groupements, identiques ou différents, choisis parmi le groupe comprenant -OH,
-000R19,
30 -002R24, et alkyle en Cl-04;
R19 est choisi parmi le groupe comprenant -(0R21R22)q_R23, un aryle en 06-012,
et un
cycloalcényle en 05-012, chaque groupe étant éventuellement substitué par un
ou plusieurs
groupements, identiques ou différents, choisis parmi le groupe comprenant un
atome
d'halogène, -OH, -000R19, -002R24, et alkyle en Cl-06; de préférence R19 est
choisi parmi
35 le groupe comprenant -(0R21R22)q_K'-'23, un aryle en 06-010, et un
cycloalcényle en 05-010,
chaque groupe étant éventuellement substitué par 1,2, 3 ou 4 groupements,
identiques ou
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
36
différents, choisis parmi le groupe comprenant un atome d'halogène, -OH, -
000R19,
-0O2R24, et alkyle en Cl-06; de préférence R19 est choisi parmi le groupe
comprenant
-(0R21K)q-R23, un aryle en 06, et un cycloalcényle en 05-08, chaque groupe
étant
éventuellement substitué par 1,2, ou 3 groupements, identiques ou différents,
choisis parmi
le groupe comprenant un atome d'halogène, -OH, -000R19, -002R24, et alkyle en
Cl-04;
q est un indice entier compris entre 3 et 12 ; de préférence q est un indice
entier compris
entre 4 et 12, par exemple q peut être 4, 5,6, 7, 8, 9, 10, 11 ou 12;
chaque R21 identique ou différent est choisi parmi H ou un alkyle en 01-06; de
préférence
chaque R21 identique ou différent est choisi parmi H ou un alkyle en Cl-04;
chaque R22 identique ou différent est choisi parmi H ou un alkyle en Cl-06; de
préférence
chaque R22 identique ou différent est choisi parmi H ou un alkyle en Cl-04;
R23 est H ou -OH, ou est choisi parmi le groupe comprenant un alkyle en Cl-06
et un aryle en
06-012, chaque groupe étant éventuellement substitué par un ou plusieurs
groupements,
identiques ou différents, choisis parmi le groupe comprenant un atome
d'halogène, -OH,
-000R19, -002R24, et alkyle en Cl-06; de préférence R23 est choisi parmi H, -
OH ou un
alkyle en Cl-04 éventuellement substitué par 1, 2 ou 3 groupements, identiques
ou
différents, choisis parmi le groupe comprenant un atome d'halogène, -OH, -
000R19,
-002R24, et alkyle en Cl-06;
R24 est H ou un alkyle en Cl-06 éventuellement substitué par un ou plusieurs
groupements,
identiques ou différents, choisis parmi le groupe comprenant -OH, -0-COR25, et
alkyle en
0l-06 de préférence R24 est H ou un alkyle en Cl-04, éventuellement substitué
par 1, 2, ou 3
groupements, identiques ou différents, choisis parmi -OH, -0-COR25, ou alkyle
en Cl-04; de
préférence R24 est H ou un alkyle en Cl-04 éventuellement substitué par 1, 2,
ou 3
groupements, identiques ou différents, choisis parmi -OH, -0-COR25, ou alkyle
en Cl-04;
R25 est choisi parmi le groupe comprenant alkyle en 02-020, et alcényle en 02-
020, chaque
groupe étant éventuellement substitué par un ou plusieurs groupements,
identiques ou
différents, choisis parmi le groupe comprenant -OH, époxy, -0R16, et -000R19;
de
préférence R25 est choisi parmi le groupe comprenant alkyle en 02-020, et
alcényle en 02-020,
chaque groupe étant éventuellement substitué par 1, 2 ou 3 groupements,
identiques ou
différents, choisis parmi le groupe comprenant -OH, époxy, -0R16, et -000R19.
L'invention concerne aussi un composé de formule (le) ou (If), un stéréo-
isomère de celui-ci,
un mélange de ceux-ci, un oligomère et/ou un polymère de ceux-ci.
Selon un mode de réalisation préféré, l'invention concerne un composé de
formule (le) ou
(If), dans lesquelles, un oligomère et/ou un polymère de ceux-ci
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
37
R16 est H ou est choisi parmi le groupe comprenant -00-(CR21R22)q_R23, -CO-
aryle en
C6-C12, et -CO-cycloalcényle en C5-C12, chaque groupe étant éventuellement
substitué par un
ou plusieurs groupements, identiques ou différents, choisis parmi le groupe
comprenant un
atome d'halogène, -OH, -000R19, -0O2R24, et alkyle en Cl-06;
R17 est un alkyle en 03-020 éventuellement substitué par un ou plusieurs
groupements,
identiques ou différents, choisis parmi un alkyle en 01-06, -0R16, ou -002R24;
de préférence
R17 est un alkyle en 03-012 éventuellement substitué par un ou plusieurs
groupements,
identiques ou différents, choisis parmi un alkyle en 01-06, -0R16, ou -002R24;
R18 est H ou un alkyle en 03-020 éventuellement substitué par un ou plusieurs
groupements,
identiques ou différents, choisis parmi un alkyle en 01-06, -0R16, ou -002R24;
de préférence
R18 est H ou un alkyle en 03-012 éventuellement substitué par un ou plusieurs
groupements,
identiques ou différents, choisis parmi un alkyle en 01-06, -0R16, ou -002R24;
ou bien R17 et R18 peuvent former, avec les carbones auxquels ils sont liés,
un groupe choisi
parmi un cycloalkyle en 05-012 ou un cycloalcényle en 05-012, chaque groupe
étant
éventuellement substitué par un ou plusieurs groupements, identiques ou
différents, choisis
parmi le groupe comprenant un atome d'halogène, -0R16, -000R19, -002R24, et
alkyle en
01-06; de préférence ou bien R17 et R18 peuvent former, avec les carbones
auxquels ils sont
liés, un groupe choisis parmi un cycloalkyle en 05-012 ou un cycloalcényle en
05-012, chaque
groupe étant éventuellement substitué par 1, 2, 3 ou 4 groupements, identiques
ou
différents, choisis parmi -OH, -000R19, -002R24, ou alkyle en 01-06;
R19 est choisi parmi le groupe comprenant -(0R21R22)q_R23, un aryle en 06-012,
et un
cycloalcényle en 05-012, chaque groupe étant éventuellement substitué par un
ou plusieurs
groupements, identiques ou différents, choisis parmi le groupe comprenant un
atome
d'halogène, -OH, -000R19, -002R24, et alkyle en 01-06; de préférence R19 est
choisi parmi
le groupe comprenant -(CR21R22)q_K'-'23, un aryle en 06, et un cycloalcényle
en 05-012, chaque
groupe étant éventuellement substitué par un ou plusieurs groupements,
identiques ou
différents, choisis parmi le groupe comprenant -OH, -000R19, -002R24, et
alkyle en 01-06;
q est un indice entier compris entre 3 et 12 ; par exemple q est 3, 4, 5, 6,
7,8, 9, 10 ou 1 1 ;
chaque R21 identique ou différent est choisi parmi H ou un alkyle en 01-06;
chaque R22 identique ou différent est choisi parmi H ou un alkyle en 01-06;
R23 est H ou -OH, ou est choisi parmi le groupe comprenant un alkyle en 01-06
et un aryle en
06-012, chaque groupe étant éventuellement substitué par un ou plusieurs
groupements,
identiques ou différents, choisis parmi le groupe comprenant un atome
d'halogène, -OH,
-000R19, -002R24, et alkyle en 01-06;
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
38
R24 est H ou un alkyle en Cl-06 éventuellement substitué par un ou plusieurs
groupements,
identiques ou différents, choisis parmi -OH, -0-COR25, ou alkyle en 01-06; et
R25 est choisi parmi le groupe comprenant alkyle en 02-020, et alcényle en 02-
020, chaque
groupe étant éventuellement substitué par un ou plusieurs groupements,
identiques ou
différents, choisis parmi le groupe comprenant -OH, époxy, -0R16, et -000R19;
à la condition que le composé ne soit pas le 9-(hexanoyloxy)-1 0-
hydroxyoctadecanoate de
méthyle, le 1 0-(hexanoyloxy)-9-hydroxyoctadecanoate de méthyle, l'ester
octanoïque de
l'hydroxyoléate de méthyle, l'ester 2-éthyl-hexyl de l'hydroxyoléate de
méthyle,
l'hydroxybenzoyloxy-octadodecanéate de méthyle, 1 ,2-heptanediol dicaproate et
le 1 ,2-
1 0 octanediol dicaproate.
Selon un mode de réalisation préféré, l'invention concerne un composé de
formule (le) ou (If)
dans lesquelles : R16 est H; et
R17 est choisi parmi le groupe contenant un alkyle en 02-020 et un alcényle en
02-020,
chaque groupe étant éventuellement substitué par un ou plusieurs groupements,
identiques
ou différents, choisis parmi un alkyle en Cl-06, un aryle en 06, OU -0R16, de
préférence R17
est choisi parmi le groupe comprenant un alkyle en 02-012 et un alcényle en 02-
020, chaque
groupe étant éventuellement substitué par 1, 2, 3 ou 4 groupements, identiques
ou
différents, choisis parmi un alkyle en 01-06, ou un aryle en 06, -0R16; de
préférence R17 est
choisi parmi le groupe comprenant un alkyle en 02-012 et un alcényle en 02-
020, chaque
groupe étant éventuellement substitué par 1, 2, 3 ou 4 groupements, identiques
ou
différents, choisis parmi un alkyle en Cl-06, ou -0R16; de préférence R17 est
un alkyle en
02-010 éventuellement substitué par 1, 2, ou 3 groupements, identiques ou
différents, choisis
parmi un alkyle en 01-04;
R18 est H ou est choisi parmi le groupe comprenant un alkyle en 02-020 et un
alcényle en
02-020, chaque groupe étant éventuellement substitué par un ou plusieurs
groupements,
identiques ou différents, choisis parmi un alkyle en 01-06, un aryle en 06, OU
-0R16; de
préférence R18 est H ou est choisi parmi le groupe comprenant un alkyle en 02-
012 et un
alcényle en 02-020, chaque groupe étant éventuellement substitué par 1, 2, 3
ou 4
groupements, identiques ou différents, choisis parmi un alkyle en 01-06, un
aryle en 06, ou
-0R16, de préférence R18 est H ou est choisi parmi le groupe comprenant un
alkyle en 02-012
et un alcényle en 02-020, chaque groupe étant éventuellement substitué par 1,
2, 3 ou 4
groupements, identiques ou différents, choisis parmi un alkyle en 01-06, ou -
0R16; de
préférence R18 est H ou un alkyle en 02-010 éventuellement substitué par 1, 2,
ou 3
groupements, identiques ou différents, choisis parmi un alkyle en Cl-04;
ou bien R16 est H ou est choisi parmi le groupe comprenant -00-(0R21R22)q_R23,
-CO-aryle
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
39
en C6-C12, et -CO-cycloalcényle en C5-C12, chaque groupe étant éventuellement
substitué par
un ou plusieurs groupements, identiques ou différents, choisis parmi le groupe
comprenant
un atome d'halogène, -OH, -000R19, -0O2R24, et alkyle en Cl-06; et R17 et R18
forment avec
les carbones auxquels ils sont liés, un groupe choisi parmi un cycloalkyle en
05-012 ou un
cycloalcényle en 05-012, chaque groupe étant éventuellement substitué par un
ou plusieurs
groupements, identiques ou différents, choisis parmi le groupe comprenant un
atome
d'halogène, -0R16, -000R19, -002R24, et alkyle en 01-06; de préférence ou bien
R17 et R18
peuvent former, avec les carbones auxquels ils sont liés, un groupe choisi
parmi un
cycloalkyle en 05-010 ou un cycloalcényle en 05-010, chaque groupe étant
éventuellement
substitué par 1, 2, 3 ou 4 groupements, identiques ou différents, choisis
parmi le groupe
comprenant un atome d'halogène, -0R16, -000R19, -002R24, et alkyle en 01-06;
de
préférence ou bien R17 et R18 peuvent former, avec les carbones auxquels ils
sont liés, un
groupe choisi parmi un cycloalkyle en 05-08 ou un cycloalcényle en 05-08,
chaque groupe
étant éventuellement substitué par 1, 2, ou 3 groupements, identiques ou
différents, choisis
parmi le groupe comprenant -OH, -000R19, -002R24, et alkyle en Cl-04;
R19 est choisi parmi le groupe comprenant -(0R21R22)q_R23, un aryle en 06-012,
et un
cycloalcényle en 05-012, chaque groupe étant éventuellement substitué par un
ou plusieurs
groupements, identiques ou différents, choisis parmi le groupe comprenant un
atome
d'halogène, -OH, -000R19, -002R24, et alkyle en 01-06; de préférence R19 est
choisi parmi
le groupe comprenant -(0R21R22)q_K'-'23, un aryle en 06-010, et un
cycloalcényle en 05-010,
chaque groupe étant éventuellement substitué par 1,2, 3 ou 4 groupements,
identiques ou
différents, choisis parmi le groupe comprenant un atome d'halogène, -OH, -
000R19,
-002R24, et alkyle en 01-06; de préférence R19 est choisi parmi le groupe
comprenant
-(0R21R22)q_R23, un aryle en 06, et un cycloalcényle en 05-08, chaque groupe
étant
éventuellement substitué par 1,2, ou 3 groupements, identiques ou différents,
choisis parmi
le groupe comprenant un atome d'halogène, -OH, -000R19, -002R24, et alkyle en
01-04;
q est un indice entier compris entre 3 et 12 ; de préférence q est un indice
entier compris
entre 4 et 12, par exemple q peut être 4, 5,6, 7, 8, 9, 10, 11 ou 12;
chaque R21 identique ou différent est choisi parmi H ou un alkyle en 01-06; de
préférence
chaque R21 identique ou différent est choisi parmi H ou un alkyle en 01-04;
chaque R22 identique ou différent est choisi parmi H ou un alkyle en 01-06; de
préférence
chaque R22 identique ou différent est choisi parmi H ou un alkyle en 01-04;
R23 est H ou -OH, ou est choisi parmi le groupe comprenant un alkyle en 01-06
et un aryle en
06-012, chaque groupe étant éventuellement substitué par un ou plusieurs
groupements,
identiques ou différents, choisis parmi le groupe comprenant un atome
d'halogène, -OH,
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
-000R19, -0O2R24, et alkyle en Cl-06; de préférence R23 est choisi parmi H, -
OH ou un
alkyle en Cl-04 éventuellement substitué par 1, 2 ou 3 groupements, identiques
ou
différents, choisis parmi le groupe comprenant un atome d'halogène, -OH, -
000R19,
-002R24, et alkyle en 01-06;
5 R24 est H ou un alkyle en Cl-06 éventuellement substitué par un ou
plusieurs groupements,
identiques ou différents, choisis parmi le groupe comprenant -OH, -0-COR25, et
alkyle en
0l-06 de préférence R24 est H ou un alkyle en Cl-04, éventuellement substitué
par 1, 2, ou 3
groupements, identiques ou différents, choisis parmi -OH, -0-COR25, ou alkyle
en Cl-04; de
préférence R24 est H ou un alkyle en Cl-04 éventuellement substitué par 1, 2,
ou 3
10 groupements, identiques ou différents, choisis parmi -OH, -0-COR25, ou
alkyle en Cl-04;
R25 est choisi parmi le groupe comprenant alkyle en 02-020, et alcényle en 02-
020, chaque
groupe étant éventuellement substitué par un ou plusieurs groupements,
identiques ou
différents, choisis parmi le groupe comprenant -OH, époxy, -0R16, et -000R19;
de
préférence R25 est choisi parmi le groupe comprenant alkyle en 02-020, et
alcényle en 02-020,
15 chaque groupe étant éventuellement substitué par 1, 2 ou 3 groupements,
identiques ou
différents, choisis parmi le groupe comprenant -OH, époxy, -0R16, et -000R19.
Selon un mode de réalisation préféré, l'invention concerne un composé de
formule (le) ou
(If), dans lesquelles,
R16 est H ou est choisi parmi le groupe comprenant -00-(0R21R22)q_R23, -CO-
aryle en
20 06-012, et -CO-cycloalcényle en 05-012, chaque groupe étant
éventuellement substitué par un
ou plusieurs groupements, identiques ou différents, choisis parmi le groupe
comprenant un
atome d'halogène, -OH, -000R19, -002R24, et alkyle en Cl-06;
R17 est un alkyle en 03-020 éventuellement substitué par un ou plusieurs
groupements,
identiques ou différents, choisis parmi un alkyle en Cl-06, -0R16, ou -002R24;
de préférence
25 R17 est un alkyle en 03-012 éventuellement substitué par un ou plusieurs
groupements,
identiques ou différents, choisis parmi un alkyle en Cl-06, -0R16, ou -002R24;
R18 est H ou un alkyle en 03-020 éventuellement substitué par un ou plusieurs
groupements,
identiques ou différents, choisis parmi un alkyle en Cl-06, -0R16, ou -002R24;
de préférence
R18 est H ou un alkyle en 03-012 éventuellement substitué par un ou plusieurs
groupements,
30 identiques ou différents, choisis parmi un alkyle en Cl-06, -0R16, ou -
002R24;
ou bien R17 et R18 peuvent former, avec les carbones auxquels ils sont liés,
un groupe choisi
parmi un cycloalkyle en 05-012 ou un cycloalcényle en 05-012, chaque groupe
étant
éventuellement substitué par un ou plusieurs groupements, identiques ou
différents, choisis
parmi le groupe comprenant un atome d'halogène, -0R16, -000R19, -002R24, et
alkyle en
35 0i-06 ; de préférence ou bien R17 et R18 peuvent former, avec les
carbones auxquels ils sont
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
41
liés, un groupe choisis parmi un cycloalkyle en C5-C12 ou un cycloalcényle en
C5-C12, chaque
groupe étant éventuellement substitué par 1, 2, 3 ou 4 groupements, identiques
ou
différents, choisis parmi -OH, -000R19, -0O2R24, ou alkyle en Cl-06;
R19 est choisi parmi le groupe comprenant -(0R21R22)q_R23, un aryle en 06-012,
et un
cycloalcényle en 05-012, chaque groupe étant éventuellement substitué par un
ou plusieurs
groupements, identiques ou différents, choisis parmi le groupe comprenant un
atome
d'halogène, -OH, -000R19, -002R24, et alkyle en 01-06; de préférence R19 est
choisi parmi
le groupe comprenant -(CR21R22)q_K'-'23, un aryle en 06, et un cycloalcényle
en 05-012, chaque
groupe étant éventuellement substitué par un ou plusieurs groupements,
identiques ou
différents, choisis parmi le groupe comprenant -OH, -000R19, -0O2R24, et
alkyle en 01-06;
q est un indice entier compris entre 3 et 12 ; par exemple q est 3, 4, 5, 6,
7,8, 9, 10 ou 1 1 ;
chaque R21 identique ou différent est choisi parmi H ou un alkyle en 01-06;
chaque R22 identique ou différent est choisi parmi H ou un alkyle en Cl-06;
R23 est H ou -OH, ou est choisi parmi le groupe comprenant un alkyle en Cl-06
et un aryle en
06-012, chaque groupe étant éventuellement substitué par un ou plusieurs
groupements,
identiques ou différents, choisis parmi le groupe comprenant un atome
d'halogène, -OH,
-000R19, -0O2R24, et alkyle en Cl-06;
R24 est H ou un alkyle en Cl-06 éventuellement substitué par un ou plusieurs
groupements,
identiques ou différents, choisis parmi -OH, -0-COR26, ou alkyle en Cl-06; et
R25 est choisi parmi le groupe comprenant alkyle en 02-020, et alcényle en 02-
020, chaque
groupe étant éventuellement substitué par un ou plusieurs groupements,
identiques ou
différents, choisis parmi le groupe comprenant -OH, époxy, -0R16, et -000R19.
La présente invention concerne aussi un oligomère et/ou un polymère de
composés de
formule (le) ou (If), tels que les composés de formule (Ig) ou (lh),
R17
16 R18
R 0 R16
0 0
R17
R1 R18 0
R19
(Ig) (lh)
dans lesquelles R16, R17, R18,
K
sont tels que décrits ci-dessus et p est un indice entier
compris entre 1 et 10 000, de préférence p est un indice entier compris entre
1 et 1000, par
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
42
exemple p est un indice entier compris entre 1 et 100.
Selon un mode de réalisation particulier, la présente invention concerne un
composé de
formule (le) ou (If) choisi parmi le groupe comprenant 9-hydroxy-10-(7-hydroxy-
3,7-
diméthyloctanoyloxy) octadecanoate de méthyle,
10-hydroxy-9-(7-hydroxy-3, 7-
diméthyloctanoyloxy) octadecanoate de méthyle, 9-(décanoyloxy)-10-
hydroxyoctadecanoate
de méthyle ; 10-(décanoyloxy)-9-hydroxyoctadecanoate de méthyle l'hexanoate de
2-
hydroxyoctyle, l'hexanoate de 1-hydroxyoctan-2-yle ; l'hexanoate de 5-
hydroxyoctan-4-yle ;
dihexanoate d'octane-4,5-diyle ; l'hexanoate de 2-hydroxycyclooctyle ;
dihexanoate de
cyclooctane-1,2-diyle ; 4-formy1-2-hydroxycyclohexyl cyclohex-3-enecarboxylate
; 5-formy1-2-
hydroxycyclohexyl 7-oxa-bicyclo[4.1.0]heptane-3-
carboxylate ; l'acide 4-(cyclohex-3-
enecarbonyloxy)-3-hydroxycyclohexanecarboxylique ; l'acide 3-(7-oxa-
bicyclo[4.1.0]heptane-
3-carbonyloxy)-4-hydroxycyclohexanecarboxylique.
Selon un mode de réalisation particulier, la présente invention concerne un
composé de
formule (la), ou (lb), susceptible d'être obtenu par le présent procédé, ayant
la formule (le)
ou (If).
Selon un mode de réalisation particulier, les composés de formule (la), (lb),
(1c), (Id), (le),
(If), (1g) ou (1h) sont utilisables dans la préparation de polymères, de
biopolymères, de
tensio-actifs, de plastifiants, ou de lubrifiants, ou dans la préparation de
polyuréthane.
Selon un mode de réalisation préféré, la présente invention concerne
l'utilisation d'un
composé de formule (la), (lb), (1c), (Id), (le), (If), (1g) ou (1h), ou du 9-
(hexanoyloxy)-10-
hydroxyoctadecanoate de méthyle, le 10-(hexanoyloxy)-9-hydroxyoctadecanoate de
méthyle, l'ester octandique de l'hydroxyoléate de méthyle, l'ester 2-éthyl-
hexyl de
l'hydroxyoléate de méthyle, l'hydroxybenzoyloxy-octadodecanéate de méthyle,
1,2-
heptanediol dicaproate et le 1,2-octanediol dicaproate ; comme monomère pour
la
préparation de polyuréthane.
Par polyuréthane, on entend les polymères issus essentiellement de la réaction
de
composés de formule (la), (lb), (1c), (Id), (le), (If), (1g) ou (1h) ou un
mélange de ceux-ci et
d'isocyanates. Par polyuréthane on entend aussi les polymères issus de la
réaction de
composés de formule (la), (lb), (1c), (Id), (le), (If), (1g) ou (1h) ou un
mélange de ceux-ci et
d'isocyanates qui contiennent, outre des fonctions uréthanes, d'autres types
de fonctions, en
particulier des cycles triisocyanuriques formés par trimérisation des
isocyanates.
L'invention concerne dès lors aussi une formulation comprenant :
- au moins un composé de formule (la), (lb), (1c), (Id), (le), (If), (1g) ou
(1h) ou un mélange de
ceux-ci, et
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
43
- au moins un isocyanate.
Ces formulations sont utilisables dans la préparation de polyuréthanes, en
particulier de
polyuréthanes thermoplastiques ou thermodurcissants. Les formulations selon
l'invention
peuvent comprendre aussi un ou plusieurs polyols classiquement utilisés pour
préparer des
polyuréthanes. On peut citer notamment les polyéther-polyols et les polyester-
polyols.
Tous les isocyanates classiquement utilisés pour fabriquer des polyuréthanes
peuvent être
mis en uvre dans l'utilisation ou les formulations selon l'invention. De
préférence
l'isocyanate est un polyisocyanate. Le polyisocyanate utilisé peut être choisi
parmi les
polyisocyanates aliphatiques, aromatiques, cycloaliphatiques et ceux qui
contiennent dans
leur molécule un cycle isocyanurate ; ayant au moins deux fonctions isocyanate
dans leur
molécule, susceptibles de réagir avec une ou plusieurs fonctions hydroxyle
d'un composé de
formule (la), (lb), (1c), (Id), (le), (If), (1g) ou (1h) pour former un réseau
polyuréthane
tridimensionnel provoquant la réticulation de la formulation.
A titre de polyisocyanates bien adapté dans la cadre de la présente invention,
on peut
notamment citer : l'hexaméthylènediisocyanate (HMDI, HDI, ou 1,6-
diisocyanatohexane), le
diphénylméthanediisocyanate (M Dl) sous la forme de ces isomères 2,4' , 2,2'
and 4,4' ou un
mélange de ceux-ci, le toluène diisocyanate (TDI), l'isophoronediisocyanate
(IPDI) , le
dicyclohexylméthanediisocyanate (DCI) ; le naphtalène 1 ,5-diisocyanate (NDI),
le p-
phénylène diisocyanate (PPDI), le 3,3'-diméthyldipheny1-4, 4'-diisocyanate
(DDDI), ou le 4,4'-
dibenzyl diisocyanate (DBDI), ou un mélange de ceux-ci.
Selon un mode de réalisation préféré, les composés de formule (la), (lb),
(1c), (Id), (le), (If),
(1g) ou (1h) sont issus du monde végétal. Les produits finaux utilisant ces
polymères sont
donc avantageusement des polymères issus du monde végétal. Le produit de la
réaction, de
préférence one pot , évoquée ci-dessus sur une huile végétale est une
molécule
fonctionnalisée en manière telle qu'elle pourra être utilisée comme matière
première à la
fabrication de matière plastique. Cette molécule est qualifiée de synthon
(building block).
Différents types de plastiques (bioplastiques) peuvent être envisagés suivant
la nature de la
fonction greffée par le procédé de synthèse.
Les exemples suivants sont donnés à titre illustratif et non limitatif de la
présente invention,
susceptibles de variantes aisément accessibles à l'homme de l'art.
Exemples
Exemple 1 :
Cet exemple montre une comparaison de différents catalyseurs constitués d'un
métal
déposé sur un support silicique. Tous les catalyseurs ont été préparés par
échange ionique
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
44
au départ d'une silice colloïdale stabilisée par des ions ammoniums et du
chlorure métallique
correspondant à l'espèce active. Ceux-ci ont été testés sur la réaction de
fonctionnalisation
de l'oléate de méthyle par l'hydroxycitronellal qui a conduit à la synthèse du
9-hydroxy-10-(7-
hydroxy-3,7-diméthyloctanoyloxy) octadécanoate de méthyle et du 10-hydroxy-9-
(7-hydroxy-
3,7-diméthyloctanoyloxy) octadécanoate de méthyle comme illustré au schéma 2.
OH
1:210CH3 OH 00CH3 00CH3
1::) OH
10CH3 1
(CH2)7 (H2C)7 OH (H2C ,õ0
2,7
+ 02 / Air
0 +
OH
0
(CH2)7 CH)
0 (CH)7 HO (CH2)7
0 7
CH3
0 èF.13 H3C
CH3
OH
Schéma 2 : fonctionnalisation de l'oléate de méthyle en présence
d'hydroxycitronellal par
époxydation et acylation successives.
La réaction a été effectuée dans un réacteur en verre de 100 ml pourvu d'une
agitation
mécanique. Une masse de 25,0 g d'ester méthylique d'huile de tournesol HTO
(haute teneur
oléique - pureté : 85 % d'oléate de méthyle) ainsi que de 13,0 g
d'hydroxycitronellal (grade
FCC - pureté : k 9 5 % - Sigma-Aldrich - ref. W258318) ont été introduites
dans le réacteur. Le
catalyseur solide du type métal supporté sur silice contient 5 % en masse de
métal et a été
ajouté au mélange réactionnel à raison de 1 % en masse de la quantité d'oléate
de méthyle
engagée soit 250 mg. Le milieu a été chauffé à 80 C sous bullage d'air
continu. Le débit d'air
a été contrôlé par un débitmètre à bille et vaut 70 ml/min. Après 7 heures de
réaction, le
débit d'air a été stoppé et le milieu réactionnel a été placé sous atmosphère
inerte (azote).
Au même moment, la température de réaction a été augmentée à 150 C. Ces
paramètres
ont été maintenus durant 5 heures supplémentaires. Des échantillons du milieu
réactionnel
ont été prélevés à intervalles réguliers afin de déterminer l'avancement de la
réaction. Les
taux de conversion des réactifs et les taux de rendement en produits désirés
après 7 et 12
heures de réaction sont listés dans le tableau 1 :
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
Tableau 1
rendement en
temps de conversion en conversion en rendement en
Type de
catalyseur produits
réaction oléate de hydroxycitronellal a époxyde a
fonctionnalisés,
(h) méthyle a (%) (%) (%)
(%)
sans catalyseur 7 37 70 27 11
12 46 92 9 24
Ru/Si02 7 75 95 52 24
12 80 100 13 39
Co/Si 02 7 76 100 31 19
12 77 100 16 29
Zn/Si02 7 66 99 30 20
12 69 100 10 27
Ni/Si02 7 51 90 34 15
12 59 98 13 25
Cr/Si02 7 49 89 31 15
12 56 97 13 25
Cu/Si02 7 34 90 24 16
12 38 97 11 22
Rh/Si02 7 34 86 18 17
12 40 96 8 26
a valeurs calculées par chromatographie gazeuse
b valeurs calculées par chromatographie d'exclusion stérique
La composition du milieu réactionnel a été déterminée par analyse
chromatographique en
5 phase gazeuse. Le chromatographe de type Agilent Technologies 6870N est
équipé d'une
colonne capillaire (SGE - BPX-70 - longueur : 30 m, diamètre interne : 0,25
mm, épaisseur
du film : 0,25pm), d'un injecteur split/splitless et d'un détecteur à
ionisation de flamme
(température de l'injecteur et du détecteur : 280 C). Le programme de
température du four a
été le suivant : 80 C (0 min) - 13 C/min - 180 C (6 min) - 13 C/min - 220 C (6
min) -
10 17 C/min - 250 C (10 min).
Les temps de rétention des différents produits dans les conditions
précédemment décrites
sont les suivants : dodécane (2,9 min) ; hydroxycitronellal (8,9 min) ; oléate
de méthyle
(12,6 mm); trans-9,10époxy-stéarate de méthyle (18,9 mm); cis-9,10-époxy-
stéarate de
méthyle (19,2 min).
15 La conversion des réactifs au temps t s'exprime comme suit : (nombre de
moles initial de
réactif- nombre de moles au temps t de réactif) / nombre de moles initial de
réactif* 100.
Le rendement en époxyde au temps t a été calculé de la manière suivante :
(nombre de
moles d'époxyde au temps t/ (nombre de moles initial d'oléate de méthyle * le
coefficient de
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
46
réponse relatif du 9,10-époxystéarate par rapport à l'oléate de méthyle) *
100.
Les produits fonctionnalisés à savoir le 9-hydroxy-10-(7-hydroxy-3,7-
dimethyloctanoyloxy)
octadecanoate de méthyle et le 10-hydroxy-9-(7-hydroxy-3,7-
dimethyloctanoyloxy)
octadecanoate de méthyle ont été analysés par chromatographie d'exclusion
stérique.
Le chromatographe Alliance 2695 de Waters est équipé d'un détecteur à indice
de réfraction
(RI 410) et de deux colonnes différentes (colonnes : Styragel - HR 0,5 et
Styragel - HR 1).
La température du four contenant les colonnes est fixée à 30 C et le
tétrahydrofurane (THF)
est utilisé comme éluant à un débit de 0,8 ml/min.
Dans ces conditions les temps de rétention ont été les suivants : produits à
haute masse
moléculaire (>1000 uma ; 15,1 mm); produits fonctionnalisés (16,2 mm); oléate
de méthyle
et 9,10-époxy-stéarate de méthyle (18,1 min) ; hydroxycitronellal (19,0 min).
Le rendement en produits fonctionnalisés est la surface relative du pic
chromatographique
exprimée en pourcent par rapport à la surface totale de tous les pics.
Exemple 2:
Cet exemple décrit la synthèse de composés fonctionnalisés au départ de
l'oléate de
méthyle. Plusieurs réactifs aldéhydiques ont été testés dont l'hexanal, le
décanal et le
benzaldéhyde. Ces trois essais ont conduit à la formation des produits
suivants :
respectivement le 9-(hexanoyloxy)-10-hydroxyoctadecanoate de méthyle et le 10-
(hexanoyloxy)-9-hydroxyoctadecanoate de méthyle dans le cas où l'hexanal est
utilisé ; le 9-
(décanoyloxy)-10-hydroxyoctadecanoate de méthyle et le 10-(décanoyloxy)-9-
hydroxyoctadecanoate de méthyle pour le décanal ; et finalement le 9-
(benzoyloxy)-10-
hydroxyoctadecanoate de méthyle et le 10-(benzoyloxy)-9-hydroxyoctadecanoate
de
méthyle lorsque le benzaldéhyde est utilisé. Ces trois réactions sont
illustrées aux schémas
3,4 et 5.
OCH3
ovOCH3 cé OOCH3 0y0CH3
7
1 CH3
CHO
(CH2)7 02! Air (C1-12)7 COOH (H
0H (H2C)7,,...0-y((H2)4
+ (CH2)4 V-
0 + (CH2)4
0
0,..1-12/7
0,eri2j7
(CH2)7 CH3
(CH2)7 CH3
CH3
(H2C)4 3 CH3
CH3
CH3
Schéma 3 : fonctionnalisation de l'oléate de méthyle en présence d'hexanal,
par époxydation
et acylation successives.
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
47
cé7OCH3OCH
cé 3 00CH3 0y0CH3
7
1
CH3
,
-1 CHO 1 COOH
(CH2)7 I , 02! Air I (H2C)70H
(H2C)7,...Ø..rr(CF12)8
( + (CH2)8 ¨ .- ,"(C112)7
I 0 + (CH2)8 ¨,,õ.
,..,),,,L, , 0
L,,,,,,L, x
I
y u-n-i217
1 me 0-n-m217
(CH2)7 CH3
(CH2)7 CH3 I
I
CH3 n il L CH
i
H3 (.H .2r...,8 ... 3 CH3
C
éH3
Schéma 4: fonctionnalisation de l'oléate de méthyle en présence de décanal par
époxydation et acylation successives.
0170CH3 CHO 0lvOCH3 COOH 010CH3
00CH3
1 0
(CH2)7 * 02/ Air
(H2C)70H . (H2C)7,70 *
( +(CH2)7
0 +
n ,
¨ (CH2)7
õ,,..,..----.,õ. ,
m., %.,r12)7
(CH2)7 (CH2)7
I I * 0 F13 I
H3
C
CH3 CH3
Schéma 5 : fonctionnalisation de l'oléate de méthyle en présence de
benzaldéhyde par
époxydation et acylation successives.
La réaction a été effectuée dans un réacteur en verre de 100 ml pourvu d'une
agitation
mécanique. Dans tous les cas, une masse de 25,0 g d'ester méthylique d'huile
de tournesol
HTO (haute teneur oléique - pureté : 85 % d'oléate de méthyle) y a été
introduite. Une
quantité d'aldéhyde a été ajoutée, celle-ci est équivalente à environ une fois
et demi le
nombre de moles d'oléate de méthyle engagée. Ainsi, pour le test en présence
d'hexanal,
une quantité égale à 7,1 g d'hexanal (pureté : 98 % - Sigma-Aldrich - ref.
115606) a été
introduite dans le réacteur. Pour le décanal, cette quantité vaut 11,2 g
(pureté : 98 % -
Sigma-Aldrich - ref. D7384) et dans le cas du benzaldéhyde, 8,6 g de
benzaldéhyde (pureté :
99 % - Sigma-Aldrich - ref. B1334) ont été ajoutés. Le catalyseur solide du
type ruthénium
sur silice, contenant 1,5 % en masse de ruthénium, a été ajouté au mélange
réactionnel à
raison de 2 % en masse de la quantité d'oléate de méthyle engagée soit 500 mg.
Ensuite, le milieu a été chauffé à 80 C sous bullage d'air continu à pression
atmosphérique.
Le débit d'air a été contrôlé par un débitmètre à bille et vaut 30 ml/min.
Dans le cas de
l'hexanal et du benzaldéhyde, après 6 heures de réaction, le débit d'air a été
stoppé et le
milieu réactionnel a été placé sous atmosphère inerte (azote). Dans le cas du
décanal, la
même opération a été effectuée après 10 heures de réaction. Dans tous les cas,
il s'agit du
temps nécessaire à la conversion totale de l'aldéhyde. Ensuite, la température
de réaction a
été augmentée à 150 C. Ces paramètres sont maintenus durant 20 heures
supplémentaires
dans le cas de l'hexanal, 15 heures pour le décanal et 9 heures pour le
benzaldéhyde. Des
échantillons du milieu réactionnel ont été prélevés à intervalles réguliers
afin de déterminer
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
48
l'avancement des réactions. La composition des différents milieux réactionnels
après chaque
étape de réaction est donnée dans le tableau 2:
Tableau 2
rendement en
conversion en conversion en rendement
temps produits
type d'aldéhyde oléate de méthyle aldéhyde
(heures) en époxyde
fonctionnai isés
(%) (%) (%)
(/o)
6 63 100 47 0
hexanal
20 76 100 11 10
92 100 45 2
décanal
25 95 100 10 7
6 100 93 56 0
benzaldéhyde
100 96 7 17
La composition du milieu réactionnel a été déterminée par analyse
chromatographique en
5 phase gazeuse. Le chromatographe de type Agilent Technologies 6870N
utilisé est tel que
décrit à l'exemple 1.
Deux programmes de température différents ont été utilisés. Le premier est le
suivant : 50 C
(5 min) - 10 C/min - 100 C (5 min) - 10 C/min - 150 C (5 min) - 10 C/min - 220
C (5 min) -
10 C/min - 250 C (5 min).
10 Celui-ci a permit notamment de détecter l'hexanal. Les temps de
rétention des différents
produits dans les conditions précédemment décrites, avec une pression en tête
de colonne
égale à 16,32 psi, ont été les suivants : hexanal (6,9 min) ; dodécane (8,1
min) ; oléate de
méthyle (30,0 min) ; trans-9,10-époxy-stéarate de méthyle (34,5 min) ; cis-
9,10-époxy-
stéarate de méthyle (34,9 min).
15 La conversion des réactifs au temps t s'exprime comme décrit à l'exemple
1. Le rendement
en époxyde au temps ta été calculé comme décrit à l'exemple 1.
Le second programme de température du four a été le suivant : 80 C (0 min) -
13 C/min -
180 C (6 min) - 13 C/min - 220 C (6 min) - 17 C/min - 250 C (10 min). Les
produits
fonctionnalisés sont détectés en fin d'analyse.
Les temps de rétention des différents produits dans les conditions
précédemment décrites
ont été les suivants : dodécane (2,9 min) ; décanal (5,2 min) ; benzaldéhyde
(5,4 min) ;
oléate de méthyle (12,6 mm); trans-9,10époxy-stéarate de méthyle (18,9 mm);
cis-
9,10-époxy-stéarate de méthyle (19,2 mm); 9-(hexanoyloxy)-10-
hydroxyoctadecanoate de
méthyle et 10-(hexanoyloxy)-9-hydroxyoctadecanoate de méthyle de méthyle (29,8
et 29,9
min) ; 9-(décanoyloxy)-10-hydroxyoctadecanoate de méthyle et 10-(décanoyloxy)-
9-
hydroxyoctadecanoate de méthyle (34,4 et 34,5 mm); 9-(benzoyloxy)-10-
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
49
hydroxyoctadecanoate de méthyle et 10-(benzoyloxy)-9-hydroxyoctadecanoate de
méthyle
(38,7 et 38,9 min).
Les rendements en produits fonctionnalisés sont calculés en attribuant un
facteur de réponse
égal à un à la surface des pics chromatographiques correspondants par rapport
à celui de
l'oléate de méthyle de départ.
Tous les produits fonctionnalisés ont été identifiés par analyse
chromatographique en phase
gazeuse couplée à un spectromètre de masse ainsi que par chromatographie
d'exclusion
stérique.
Exemple 3:
Cet exemple décrit la synthèse de composés fonctionnalisés au départ
d'hexanal. Plusieurs
composés insaturés ont été testés dont le 1-octène, le 4-octène et le
cyclooctène. Ces trois
essais ont conduits à la formation de l'hexanoate de 2-hydroxyoctyle,
l'hexanoate de 1-
hydroxyoctan-2-yle et du dihexanoate d'octane-1,2-diyle dans le cas de la
réaction du 1-
octène avec l'hexanal ; l'hexanoate de 5-hydroxyoctan-4-yle et le dihexanoate
d'octane-4,5-
diyle lorsque le 4-octène est utilisé ; l'hexanoate de 2-hydroxycyclooctyle et
le dihexanoate
de cyclooctane-1,2-diyle pour le cyclooctène. Ces trois réactions sont
illustrées aux schémas
6,7 et 8.
pH3
(H2C)5 H3C% H3C,
)¨OH (CH2)5 (CH2)5
(CH2)51-H3C\(J0
02 / Air 0-Ç
2E)14
(CH2)5 + H3C, ,COOH¨> 0 + + C) '0,e0
CH3 CH3 (CH2)4(CH2)4 (CH2)4
(CH2)4 H3d H3d
(CH2)4
H
H3d 3d
Schéma 6: schéma de la fonctionnalisation du 1-octène en présence d'hexanal
par
époxydation et acylation successives.
9H3 CH3 CH3 CH3
(CH2)4 u
(CH2)2 (CH2)2
+
02 / Air N H3C, ,COOH
N11, H3C, (61-?:)4C) ,0 (CH2)4 0 0
(CH2)2 (,H2)2
H 0-----.."'.'(C1-92)2 (CH2)4 0(CH2)2
I
CH3 CH3
CH3
Schéma 7: schéma de la fonctionnalisation du 4-octène en présence d'hexanal
par
époxydation et acylation successives.
CA 02813286 2013-03-28
WO 2012/055946
PCT/EP2011/068824
?H3
(:),(cH2)4
e, CH
H C O 02 / Air H3C, ,CO
OH o.
3,(c,2)4 + (CH2)4OH +
____________________________________________________________________________
0 0
7L0
/L0
(CH2)4
(CH2)4
CH3
CH3
Schéma 8: schéma de la fonctionnalisation du cyclooctène en présence d'hexanal
par
époxydation et acylation successives.
La réaction a été effectuée dans un réacteur en verre de 100 ml pourvu d'une
agitation
5 mécanique. Dans les trois cas, une masse de 15,0 g du composé insaturé a
été introduite
dans le réacteur. Dans le premier, le 1-octène (Sigma-Aldrich ¨ pureté : 98% -
lot.
0001452135), le second le 4-octène (Sigma-Aldrich ¨ pureté : 90% - lot.
10325JE) et le
dernier le cyclooctène (Sigma-Aldrich ¨ pureté : 95% - lot. 7238917). Ensuite,
20,5 g
d'hexanal (Sigma-Aldrich - pureté : 98 % - lot. S88145-279) ont été
introduites dans chaque
10 réacteur ainsi que 300 mg de catalyseur solide du type ruthénium sur
silice, contenant 1,5 %
en masse de ruthénium. Le milieu a été chauffé à 80 C sous bullage d'air
continu. Le débit
d'air a été contrôlé par un débitmètre à bille et vaut 30 ml/min. Après 7
heures de réaction, le
débit d'air a été stoppé et le milieu réactionnel a été placé sous atmosphère
inerte (azote).
Au même moment, la température de réaction a été augmentée à 120 C. Ces
paramètres
15 ont été maintenus durant 15 heures supplémentaires de manière générale et
durant 70
heures dans le cas du 4-octène. Des échantillons du milieu réactionnel ont été
prélevés à
intervalles réguliers afin de déterminer l'avancement de la réaction. La
composition des
différents milieux réactionnels après chaque étape de réaction est donnée dans
le tableau 3
tandis que les courbes cinétiques de conversion en réactifs et de rendement en
produits
20 dans le cas du 4-octène sont reprises dans le graphique de la Figure 1 :
Tableau 3
rendement en rendement
en
conversion conversion rendement
temps produits produits
type d'oléfine en oléfine en hexanal en époxyde
(heures) (% (% (%
fonctionnalisés difonctionnalisés
) ) )
(/o)
(/o)
7 78 100 10 3 6
1-octène
22 90 100 0 7 5
7 84 100 51 2 0
4-octène 22 96 100 27 26 2
77 100 100 0 10 10
7 100 100 74 4
n.d.
cyclooctène
22 100 100 69 3
n.d.
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
51
La composition quantitative des différents milieux réactionnels a été
déterminée par analyse
chromatographique en phase gazeuse. Le chromatographe de type Agilent
Technologies
6870N utilisé est tel que décrit à l'exemple 1.
Le programme de température du four a été le suivant : 50 C (5 min) - 10 C/min
- 100 C (5
min) - 10 C/min - 150 C (5 min) - 10 C/min - 220 C (5 min) - 10 C/min - 250 C
(5 min).
Les temps de rétention des différents produits dans les conditions
précédemment décrites,
avec une pression en tête de colonne égale à 16,32 psi, ont été les suivants :
4-octène (2,9
mm); 1-octène (2,9 mm); cyclooctène (5,1 mm); hexanal (6,9 mm); dodécane (8,1
mm);
4,5-époxyoctane (8,1 mm); 1,2-époxyoctane (9,6 mm); époxycyclooctane (15,8
min) ;
hexanoate de 5-hydroxyoctan-4-yle (26,6 mm); dihexanoate d'octane-4,5-diyle
(29, 0 mm);
dihexanoate d'octane-1,2-diyle (30,3 mm); hexanoate de 2-hydroxyoctyle et
hexanoate de 1-
hydroxyoctan-2-yle (29,7 et 31,6 min) ; hexanoate de 2-hydroxycyclooctyle
(31,9 min).
La conversion des réactifs au temps t s'exprime comme décrit à l'exemple 1. Le
rendement
en produit époxydé au temps t a été calculé de la manière suivante : (nombre
de moles du
produit au temps t/ (nombre de moles initial du réactif correspondant * le
coefficient de
réponse relatif du produit par rapport au réactif) * 100.
Les rendements des composés fonctionnalisés sont calculés de la même manière
mais en
attribuant un coefficient de réponse égale à un.
Tous les produits fonctionnalisés ont été identifiés par analyse
chromatographique en phase
gazeuse couplée à un spectromètre de masse.
Exemple 4:
Cet exemple concerne la synthèse de molécules fonctionnalisées à partir de
composé de
formule (II) et (III) qui sont les mêmes, la molécule utilisée le 3-
cyclohexène-1-
carboxaldéhyde comportant les deux fonctionnalités insaturation et aldéhyde.
Les réactions
d'époxydation et d'acylation successives sur cette molécule ont conduit tout
d'abord à la
production de l'intermédiaire époxy-acide et ensuite à la formation des
dimères, des trimères
et des oligomères du composé de départ comme l'illustre le schéma 9.
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
52
0 Ifli
i 0 à
7H
C Ci HO'll HO r,Zif ir,Zif
C1F1 rYOH
Ciç
02 t Air (7
_Q
-I...-
O 3H O C:OH
OLIGOMERES
i0f)H
Y c:,-1H021D HO
0 C)
o
REACTIF MONOMERES DIMERES
Schéma 9: fonctionnalisation du 3-cyclohexène-1-carboxaldéhyde par époxydation
et
acylation successives.
La réaction a été effectuée dans un réacteur en verre de 100 ml pourvu d'une
agitation
mécanique. Une masse de 30,0 g de 3-cyclohexène-1-carboxaldéhyde (Sigma-
Aldrich ¨
pureté : 97% - lot. MKBD1569) a été introduite dans le réacteur. Le catalyseur
solide du type
ruthénium sur silice, contenant 1,5 % en masse de ruthénium, a été ajouté au
mélange
réactionnel à raison de 1 % en masse de la quantité de réactif engagée soit
300 mg. Le
milieu a été chauffé à 80 C sous bullage d'air continu. Le débit d'air a été
contrôlé par un
débitmètre à bille et vaut 70 ml/min. La réaction a été menée durant 14 heures
sans le
remplacement de l'air par de l'azote. La température de réaction a été
maintenue durant
toute la durée de l'essai à 80 C. Des échantillons du milieu réactionnel ont
été prélevés à
intervalles réguliers afin de déterminer l'avancement de la réaction. Dans ce
cas,
l'avancement de la réaction a été déterminé par chromatographie d'exclusion
stérique. Les
résultats sont présentés sont la forme d'un graphique reprenant les courbes
cinétiques de
l'avancement de la réaction à la Figure 2.
La composition du milieu réactionnel a été déterminée par chromatographie
d'exclusion
stérique. Le chromatographe Alliance 2695 de Waters a été équipé d'un
détecteur à indice
de réfraction (RI 410) et de deux colonnes différentes (colonnes : Styragel -
HR 0,5 et
Styragel - HR 1). La température du four contenant les colonnes est fixée à
30 C et le
tétrahydrofurane (THF) est utilisé comme éluant à un débit de 0,8 ml/min.
Une courbe de calibration a été tracée à l'aide de standards de polystyrène
sur base de la
mesure du signal du détecteur à indice de réfraction. Ces standards sont
composés de
polymères de styrène de masse moléculaire connue. Cette courbe de calibration
a été tracée
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
53
sur un graphique portant le logarithme en base dix de la masse molaire en
fonction du temps
de rétention. Ainsi, les différents produits de la réaction ont pu être
identifiés par la mesure
de leur masse moléculaire respective.
Dans les conditions d'analyse décrites ci-dessus, les temps de rétention ont
été les
suivants : le terme monomères repris dans le graphique de la Figure 2
comprend le
réactif et les produits monomériques de la réaction ; le 3-cyclohexène-1-
carboxaldéhyde
(22,84 min), l'acide 3-cyclohexène-1-carboxylique (21,54 min), le 3,4-
époxycyclohexane-1-
carboxaldéhyde (21,54 min) et l'acide 3,4-époxycyclohexane-1-carboxylique
(20,90 min). Le
terme dimères inclus tous les composés dimériques (19,63 + 19,13 + 18,63
min).
Finalement, le terme trimères et oligomères reprend les composés à plus
haute masse
moléculaire (18,32 + 17,75 min).
La quantification a été effectuée sur la base du signal du détecteur à indice
de réfraction en
attribuant à tous les composants du milieu réactionnel un coefficient de
réponse égal à un.
C'est donc la proportion, en terme de surface de pic, de chacun d'eux (ou par
groupe de
pics) par rapport à la surface totale de tous les pics qui a été calculée.
Exemple 5
Cet exemple décrit la synthèse d'un polyuréthane thermoplastique obtenu au
départ d'un diol
synthétisé par le procédé dont fait l'objet l'invention. Le diol dont il est
question est
entièrement biosourcé et provient de la réaction entre l'oléate de méthyle et
l'hydroxycitronellal. L'application du procédé sur ces deux réactifs conduit à
la synthèse du
9-hydroxy-10-(7-hydroxy-3,7-diméthyloctanoyloxy) octadécanoate de méthyle et
du 10-
hydroxy-9-(7-hydroxy-3,7-diméthyloctanoyloxy) octadécanoate de méthyle comme
illustré
dans l'exemple n 1. Ces deux molécules sont des isomères de position et
représente la
source de diol pour la fabrication du polyuréthane, la source de diisocyanate
étant le 1,6-
diisocyanatohexane (HM Dl).
La réaction de fonctionnalisation de l'oléate de méthyle a été réalisée dans
un réacteur
fermé pourvu d'une agitation mécanique, sous pression d'oxygène pur et en
l'absence de
solvant. Une masse de 10,0 g d'oléate de méthyle (Sigma Aldrich - pureté : 99
% - ref.
311111) ainsi que de 29,0 g d'hydroxycitronellal (grade FCC - pureté : k 9 5 %
- Sigma-
Aldrich - ref. W258318) ont été introduites dans le réacteur. Le catalyseur
solide du type
métal supporté sur silice contient 1,5 % en masse de métal et a été ajouté au
mélange
réactionnel à raison de 2 % en masse de la quantité d'oléate de méthyle
engagée soit 200
mg. Le milieu a été chauffé à 70 C et de l'oxygène y a été introduit jusqu'à
une pression de 4
bars. Cette pression a été maintenue constante par des ajouts réguliers
d'oxygène. La
réaction d'époxydation, première étape du procédé monotope, s'est terminée
après 2 heures
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
54
(plus aucune consommation d'oxygène). A ce moment, le rendement en époxyde
était de 90
% avec une sélectivité de 95 % (évaluée par chromatographie gazeuse suivant la
méthode
décrite dans l'exemple n 1). Ensuite, le réacteur a été ramené à la pression
atmosphérique,
le milieu réactionnel a été dégazé et l'oxygène résiduel a été chassé par de
l'azote. La
température a été augmentée à 120 C et la deuxième étape du procédé monotope a
débuté,
la réaction d'ouverture de l'époxyde. Cette étape a été beaucoup plus lente et
a nécessité 48
heures.
La réaction de fonctionnalisation terminée, l'excès d'acide citronellique
présent dans le milieu
réactionnel a été éliminé par extraction liquide-liquide. Le milieu
réactionnel a été dilué dans
l'éther diéthylique puis centrifugé afin d'éliminer le catalyseur solide. La
phase organique
éthérée a été ensuite placée dans une ampoule à décanter et une solution
aqueuse de
NaOH, ayant une concentration égale à 0,3 M, y a été ajoutée. Plusieurs
lavages successifs
de la phase organique ont été opérés avec la solution basique pour terminer
par une solution
à 0,05 M en HCI. Finalement, un dernier lavage a été effectué avec une
solution saturée en
NaCI jusqu'à fin d'acidité. La phase organique a été finalement séchée avec du
carbonate de
sodium et l'éther diéthylique a été évaporé via un évaporateur rotatif. A ce
moment, le milieu
réactionnel était constitué à 72 % du produit d'ouverture (diol) d'après
l'analyse en
chromatographie d'exclusion stérique (méthode d'analyse décrite dans l'exemple
n 1).
La réaction de polymérisation a été également menée sous atmosphère inerte
(azote). Le
diol obtenu dans l'étape précédente a été chauffé à 120 C et le 1,6-
diisocyanatohexane a
été ajouté en quantité hémi-molaire par rapport au diol. Après 2 heures de
réaction, la
température a été amenée à 150 C et une quantité de diisocyanate a été ajouté
afin que la
quantité totale soit équimolaire par rapport au diol. La réaction a été
poursuivie durant 2
heures supplémentaires.
Afin de démontrer la formation d'un polyuréthane, deux techniques analytiques
ont été mises
en uvre : la chromatographie d'exclusion stérique et la spectrométrie
infrarouge. La
première a permit de mettre en évidence l'évolution de la masse molaire du
produit, la
seconde a permit de visualiser la formation des liens uréthanes.
Les analyses de chromatographie d'exclusion stérique ont été effectuée à
l'aide d'un
chromatographe Alliance 2695 de Waters équipé d'un détecteur à indice de
réfraction (RI
410) et de trois colonnes différentes (colonnes : Styragel - HR 0,5 - HR 1 ¨
HR 3). La
température du four contenant les colonnes a été fixée à 30 C et le
tétrahydrofurane (THF) a
été utilisé comme éluant à un débit de 0,8 ml/min.
Une courbe de calibration, portant le logarithme de la masse molaire de
standards de
polystyrène en fonction du temps de rétention, a été établie. Quatre standards
ayant une
CA 02813286 2013-03-28
WO 2012/055946
PCT/EP2011/068824
masse moléculaire connue et une structure moléculaire proche de celle du
produit de
fonctionnalisation dont il est question ont été analysés afin de déterminer le
facteur correctif.
La première partie du tableau 4 ci-dessous reprend les résultats d'analyse du
produit
fonctionnalisé avant la polymérisation et la seconde partie du tableau, les
résultats obtenus à
5 la fin de l'étape de polymérisation.
Tableau 4
Temps de Masse Masse
rétention % Aire des pics moléculaire moléculaire
(min) mesurée corrigée
27.411 71.99 830 538
avant 28.538 12.97 564 388
polymérisation 29.680 12.07 418 301
31.703 2.97 284 217
19.312 5.05 120324 35946
20.549 19.52 18012 7229
22.359 35.51 5313 2578
23.987 13.56 2961 1574
après 4 heures
25.125 5.53 1989 1124
26.104 7.79 1372 822
27.749 5.43 734 485
29.743 7.62 412 298
Le mélange de départ contient environ 70% du produit fonctionnalisé. Après la
réaction de
polymérisation, les oligomères les plus représentés contiennent de 5 à 10
unités
monomériques avec environ 5% d'oligomère contenant 50 unités. Des chaines
polymériques
10 plus longues sont aussi probablement présentes.
La figure 3 montre les spectres infrarouges du produit fonctionnalisé en
présence de
diisocyanate avant polymérisation (t = 0 min) et après polymérisation (t=240
min).
On observe la disparition de la bande d'absorption du lien O-H vers 3400cm-1
au profit de la
bande du lien N-H de l'amine secondaire vers 3350 cm-1. La disparition du pic
caractéristique
15 des isocyanates entre 2300 et 2200 cm-1 montre la conversion de ces
derniers.
L'augmentation de l'intensité de la bande d'absorption C=0 des esters entre
1730 et 1715
cm-1 est due à la contribution des doubles liens C=0 des fonctions uréthanes.
Finalement, on
observe l'apparition des pics à 1520cm-1 et 1250cm-1 caractéristiques des
liens uréthanes.
Exemple 6:
20 Cet exemple décrit la synthèse d'un polyuréthane thermodurcissant obtenu au
départ de
l'huile de soja fonctionnalisée. Le polyol obtenu par fonctionnalisation de
l'huile de soja en
présence de butyraldéhyde a été utilisé pour la fabrication du polyuréthane,
le diisocyanate
étant le 1,6-diisocyanatohexane (HM Dl).
CA 02813286 2013-03-28
WO 2012/055946
PCT/EP2011/068824
56
La réaction de fonctionnalisation a été réalisée dans un réacteur fermé pourvu
d'une
agitation mécanique, sous pression d'oxygène pur et en l'absence de solvant.
Une masse de
10,0 g d'huile de soja raffinée (indice d'iode : 112,5 g I2/100g) ainsi que de
30,0 g de
butyraldéhyde (Sigma-Aldrich - pureté : 99 % - ref. 538191) ont été introduits
dans le
réacteur. Le catalyseur solide du type métal supporté sur silice contient 1,5
% en masse de
métal et a été ajouté au mélange réactionnel à raison de 2 % en masse de la
quantité
d'oléate de méthyle engagée soit 200 mg. Le milieu a été chauffé à 70 C et de
l'oxygène y a
été introduit jusqu'à une pression de 4 bars. Cette pression a été maintenue
constante par
des ajouts réguliers d'oxygène. La réaction d'époxydation, première étape du
procédé
monotope, s'est arrêtée après 4 heures (plus aucune consommation d'oxygène).
Ensuite, le
réacteur a été ramené à la pression atmosphérique, le milieu réactionnel a été
dégazé et
l'oxygène résiduel a été chassé par de l'azote. La température a été augmentée
à 120 C et
la deuxième étape du procédé monotope a débuté, c'est la réaction d'ouverture
de l'époxyde
qui a nécessité 48 heures.
La réaction de fonctionnalisation terminée, l'excès d'acide butyrique présent
dans le milieu
réactionnel a été éliminé par extraction liquide-liquide suivant le protocole
décrit dans
l'exemple n 5.
La réaction de polymérisation a été menée sous atmosphère inerte (azote). Le
polyol obtenu
dans l'étape précédente a été chauffé à 100 C et le 1,6-diisocyanatohexane a
été ajouté en
très petite quantité afin de provoquer la réaction de polymérisation tout en
gardant le
mélange dans un état liquide nécessaire pour les analyses chromatographique et
spectrométrique.
Les analyses de chromatographie d'exclusion stérique ont été menées suivant le
protocole
de l'exemple n 5. La première partie du tableau 5 ci-dessous reprend les
résultats d'analyse
du produit fonctionnalisé avant la polymérisation et la seconde partie du
tableau, les résultats
obtenus après une polymérisation partielle (l'échantillon thermodur n'étant
pas soluble dans
le THF).
Tableau 5
Temps de Masse Masse
rétention % Aire des pics moléculaire
moléculaire
(min) mesurée corrigée
22.729 23.02 4580 2274
avant
23.501 19.62 3486 1806
polymérisation
25.075 57.37 2026 1142
CA 02813286 2013-03-28
WO 2012/055946
PCT/EP2011/068824
57
Temps de Masse Masse
rétention % Aire des pics moléculaire
moléculaire
(min) mesurée corrigée
19.196 22.01 154860 44484
20.346 20.14 22620 8763
après 30
22.273 18.23 5513 2660
minutes
23.301 12.57 3731 1913
25.115 27.04 1996 1128
Le mélange de départ contient environ 77 % de l'huile fonctionnalisée, celle-
ci pouvant
contenir jusqu'à 9 fonctions butyranoate. Après la réaction de polymérisation
partielle, les
oligomères les plus représentés contiennent jusqu'à 32 unités monomériques. A
ce stade, il
reste encore environ 40 % de monomères mais au-delà de cette proportion, le
mélange
devient solide et non analysable. Pour une polymérisation totale, il est
évident que les
masses molaires sont plus élevées que celles annoncés.
La figure 4 ci-dessous montre les spectres infrarouges du produit
fonctionnalisé avant
polymérisation (t = 0 min) et après polymérisation (t = 30 min).
On observe une atténuation de la bande d'absorption du lien 0-H vers 3475 cm-1
au profit de
la bande du lien N-H de l'amine secondaire vers 3400 cm-1. On observe
également
l'apparition des pics à 1520 cm-1 et 1250 cm-1 caractéristiques des liens
uréthanes.
Exemple 7:
Cet exemple illustre l'utilisation d'un catalyseur pour la seconde étape du
procédé monotope
entre l'oléate de méthyle et l'hexanal afin de former le 9-(hexanoyloxy)-10-
hydroxyoctadecanoate de méthyle et le 10-(hexanoyloxy)-9-hydroxyoctadecanoate
de
méthyle. Les catalyseurs testés sont :
des catalyseurs solides acides. Une résine polymérique du type Amberlyst 15
(A15)
fonctionnalisée par des fonctions sulfoniques (résine acide fort) et quatre
montmorillonites différentes : une montmorillonite (M) possédant une surface
spécifique de 330 m2/g et un PZC (point of zero charge) de 2,8-3,8; une
seconde
(MAI) dont la surface spécifique vaut 250 m2/g et le PZC vaut entre 4 et 5;
une
troisième (MK10) possédant une surface spécifique de 250 m2/g et un PZC de
3,6; et
la dernière (MKSF) ayant une surface spécifique comprise entre 20 et 40 m2/g.
des catalyseurs solides basiques. Deux résines polymériques Amberlyst , l'une
de
type 21 (A21) fonctionnalisée par des alkyles amines (résine base faible) et
l'autre de
type 26 (A26) fonctionnalisée par des ammoniums quaternaires (résine base
forte).
L'oxyde de calcium (CaO) a également été testé ainsi qu'une hydrotalcite
synthétique
(Mg6Al2(CO3)(OH)16 4 H20).
CA 02813286 2013-03-28
WO 2012/055946 PCT/EP2011/068824
58
des catalyseurs homogènes. Il s'agit de l'hexylamine, la dihexylamine, la
trihexylamine
et l'hydroxyde de potassium.
Chaque réaction a été effectuée dans un réacteur en verre de 100 ml pourvu
d'une agitation
mécanique. Dans tous les cas, une masse de 20,0 g d'ester méthylique d'huile
de colza
(pureté : 60 % d'oléate de méthyle) ainsi que de 10,2 g d'hexanal (pureté : 98
% - Sigma-
Aldrich - ref. 115606) ont été introduits dans le réacteur. Le catalyseur
solide du type métal
supporté sur silice contient 1,5 % en masse de ruthénium et a été ajouté au
mélange
réactionnel à raison de 1 % en masse de la quantité d'ester méthylique engagée
soit 200
mg.
Ensuite, le milieu a été chauffé à 80 C sous bullage d'oxygène pur à pression
atmosphérique. Le débit d'air a été contrôlé par un débitmètre à bille et
valait 10 ml/min.
Après 7 heures de réaction, la conversion en oléate de méthyle était de 89
(:)/0, la conversion
en hexanal était de 96 % et le rendement en époxyde était de 72 %. A ce
moment, le débit
d'air a été stoppé et le milieu réactionnel a été placé sous atmosphère inerte
(azote). Le
milieu réactionnel a été maintenu à 80 C et le catalyseur d'ouverture a été
ajouté à raison
de 5 % en masse pour les catalyseurs solides et de 50p1 dans le cas des
hexylamines. En ce
qui concerne l'hydroxyde de potassium, 50p1 d'une solution méthanolique d'une
concentration de 0,5M ont été ajoutés. Le milieu a été maintenu sous agitation
durant 24
heures supplémentaires.
La figure 5 reprend sous la forme d'un graphique, portant la sélectivité en
produits
fonctionnalisés en fonction du rendement, les résultats obtenus au terme de la
réaction
monotope, après 31 heures de réaction.
La composition du milieu réactionnel a été déterminée par analyse
chromatographique en
phase gazeuse suivant le protocole décrit dans l'exemple n 2.